Sistema motorio somatico e sistema nervoso
Sistema motorio somatico e sistema nervoso
Questo sito utilizza cookie, anche di terze parti. Se vuoi saperne di più leggi la nostra Cookie Policy. Scorrendo questa pagina o cliccando qualunque suo elemento acconsenti all’uso dei cookie.I testi seguenti sono di proprietà dei rispettivi autori che ringraziamo per l'opportunità che ci danno di far conoscere gratuitamente a studenti , docenti e agli utenti del web i loro testi per sole finalità illustrative didattiche e scientifiche.
Le informazioni di medicina e salute contenute nel sito sono di natura generale ed a scopo puramente divulgativo e per questo motivo non possono sostituire in alcun caso il consiglio di un medico (ovvero un soggetto abilitato legalmente alla professione).
Sistema motorio somatico e sistema nervoso
SISTEMA NERVOSO
Il sistema motorio somatico
La motilità delle fibre scheletriche dipende da diversi livelli di controllo motorio che prendono il nome di sottosistemi motori.
Il primo sottosistema motorio è costituito dai motoneuroni inferiori. Si tratta dei motoneuroni α del corno anteriore della sostanza grigia del midollo spinale e dei neuroni motori dei nervi cranici. La loro attività dipende dai circuiti nervosi situati nel midollo spinale e nel tronco encefalico, responsabili dei riflessi, e dai motoneuroni superiori.
Il secondo sottosistema motorio è formato dai motoneuroni superiori. Comprende strutture del tronco encefalico e della corteccia motoria, premotoria e motoria supplementare. Il tronco encefalico controlla la postura ed i movimenti grossolani tramite le vie reticolo-spinale, vestibolo-spinale, tetto-spinale e rubro-spinale. La corteccia invece si serve di una via diretta – cortico-spinale – per il controllo dei movimenti fini, e di vie indirette che si arrestano nel tronco encefalico.
Il terzo sottosistema motorio è quello del cervelletto. Esso agisce tramite la corteccia ed il tronco encefalico. Tra le sue funzioni vi è quella di correggere gli errori motori.
Il quarto sottosistema motorio è quello dei gangli della base. Essi agiscono attraverso la corteccia e il tronco encefalico. La loro funzione è complessa, ed ancora non del tutto chiara.
Il sottosistema motorio dei motoneuroni inferiori
Omeostasi. Secondo la definizione data nel 1929 da Cannon, l'omeostasi è la capacità di mantenere costanti i parametri dell'ambiente interno, al fine di preservare la normale funzione delle cellule. L'omeostasi è dunque la capacità di mantenere costanti i fattori che influenzano l'attività cellulare (osmolarità, temperatura, pH) e di procurare il materiale di cui la cellula ha bisogno: acqua, ossigeno, sodio, calcio.
Le proprietà dell'omeostasi sono definite dai postulati di Cannon:
- il SN ha un ruolo nel mantenimento dell'adeguatezza dell'ambiente interno (volume ematico, pressione arteriosa, temperatura corporea, osmolarità)
- può esistere un livello tonico di attività: un fattore può avere un'attività moderata che può essere fatta aumentare o diminuire dai controlli omeostatici (es. calibro vasale)
- può esistere un controllo antagonista, se due fattori agiscono sullo stesso parametro in modo opposto (è il caso di insulina e glucagone)
- i segnali chimici possono avere effetti diversi nei diversi tessuti del corpo (l'adrenalina è vasocostrittrice o vasodilatatrice a seconda della presenza di recettori α o β)
L'omeostasi richiede un continuo controllo di numerosi parametri e coordinazione nelle risposte. Ciò viene ottenuto grazie a due tipi di controlli:
- controllo locale
- riflessi
Il controllo locale è limitato alla zona in cui si verifica il cambiamento. La cellula sente il cambiamento e risponde liberando una sostanza che si oppone a tale cambiamento, in modalità autocrina o paracrina. Né è un esempio l'ipossia locale, che porta alla liberazione per via paracrina di acido lattico, sostanza vasodialtante.
Il riflesso è situato all'esterno dell'organo o della cellula che attua la risposta. I riflessi utilizzano il sistema nervoso, il sistema endocrino o entrambi. La finalità del riflesso è quella di rimuovere lo stimolo a cui è sensibile. L'organizzazione schematica di un riflesso è la seguente:
STIMOLO
![]()
SENSORE
VIA AFFERENTE
CENTRO INTEGRATORE
![]()
![]()
VIA EFFERENTE
EFFETTORE
RISPOSTA
Nei riflessi neuroendocrini esistono due centri integratori: lo stimolo viene portato attraverso la via afferente all'ipotalamo (I centro di integrazione), poi la via efferente si porta all'ipofisi (II centro di integrazione), infine sia ha la risposta da parte degli effettori.
L'arco riflesso è il circuito nervoso che determina il riflesso.
La caratteristica generale dei riflessi è quella di scatenare una risposta
- incosciente
- stereotipata
- atta a rimuovere la causa del riflesso
Classificazione dei riflessi. I riflessi possono essere classificati in base a:
- via efferente motoria
- somatici
- viscerali
- centro di integrazione
- spinali
- tronco encefalici
- corticali
- numero di neuroni coinvolti
- monosinaptici
- polisinaptici
- richiesta o meno di esperienza
- innati
- condizionati
Riflessi spinali.
I riflessi spinali sono integrati a livello del midollo spinale; sono presenti anche nel paziente tetraplegico. Tra i riflessi spinali ricordiamo
- il riflesso da stiramento
- il riflesso inverso da stiramento
- il riflesso della deambulazione
- riflessi viscerali, come quelli della defecazione, della minzione e sessuali
Riflesso da stiramento muscolare (o miotatico).
Si tratta di un riflesso fondamentale anche per i movimenti volontari.
Stimolo: allungamento del muscolo scheletrico (es. percussione del tendine patellare)
Recettore: fuso neuromuscolare
Via afferente: neurone sensitivo che innerva il fuso neuromuscolare
Centro di integrazione: motoneurone α
Via efferente: motoneurone α
Effettori: muscolo scheletrico
Risposta: contrazione muscolare
Lo scopo è quello di mantenere costante la lunghezza del muscolo. È da ricordare che il ramo centripeto del neurone a T emette dei rami collaterali che innervano neuroni inibitori dei motoneuroni dei muscoli antagonisti.
Fusi neuromuscolari. I sensori di lunghezza nel riflesso miotatico sono i fusi neuromuscolari. Sono delle strutture fusiformi, situate tra le fibre muscolari scheletriche, in parallelo ad esse. I fusi sono circondati da una capsula connettivale e si inseriscono sull'endomisio o sui tendini. Ciascun fuso contiene fibre muscolari scheletriche diverse dalle fibre extrafusali. La parte centrale del fuso è cedevole e contiene meno fibre contrattili. La parte periferica è contrattile, essendo più ricca in elementi contrattili. Le fibre contrattili fusali sono di due tipi: le fibre a scacco nucleare e le fibre a catena nucleare. Le fibre a sacco nucleare sono più grosse e contengono multi nuclei nella parte centrale (sacco d'arance), e sono in numero di 2 per ogni fuso. Le fibre a catena nucleare – più fini – sono in numero di 4 per fuso e si inseriscono sulle estremità delle fibre a sacco nucleare.
Anche le terminazioni nervose sono di due tipi: terminazioni anulospirali e terminazioni a fiorami. Le terminazioni anulospirali sono terminazioni di fibre a conduzione rapida (Ia) ed avvolgono la parte centrale di tutte le fibre intrafusali. Le terminazioni a fiorami sono terminazioni di fibre più lente (II) e terminano vicino alle estremità delle sole fibre a catena nucleare. I fusi, con le loro fibre afferenti, producono due tipi di risposta, dinamica e statica.
I fusi neuromuscolari hanno anche un'innervazione motoria loro propria, costituita da fibre motorie sottili, costituite dai cosiddetti motoneuroni γ. Alcuni motoneuroni di dimensioni maggiori (motoneuroni β) innervano sia le fibre intrafusali che quelle extrafusali.
Quando il muscolo viene allungato, le terminazioni nervose vengono distorte e generano potenziali d'azione. Le fibre afferenti provenienti da terminazioni a fiorami sono responsabili della risposta statica. Anche in condizioni di riposo i muscoli hanno una certa lunghezza, per cui le fibre intrafusali sono stimolate con bassa frequenza e scaricano a loro volta a bassa frequenza in modo tonico, provocando una leggera contrazione muscolare tonica, il tono muscolare. Le terminazioni anulospirali, invece, sono molto più sensibili alle variazioni di lunghezza del fuso: esse scaricano con una frequenza maggiore quando il muscolo viene stirato (risposta dinamica).
Le fibre efferenti γ hanno una funzione diversa dalle fibre α: la loro stimolazione, infatti, non è sufficiente per far contrarre il muscolo. Quando le fibre γ si contraggono, il risultato è una deformazione delle terminazioni nervose anulospirali e a fiorami, con conseguente aumento della scarica delle fibre afferenti. Le fibre γ sono divise in due gruppi, γ-statiche e γ-dinamiche, che innervano rispettivamente le fibre a catena nucleare e le fibre a sacco nucleare. La stimolazione di un gruppo solo di fibre aumenta solo un tipo di risposta, statica o dinamica, influendo poco sull'altro tipo.
Quando il muscolo si contrae volontariamente, all'attivazione delle fibre α corrisponde anche una attivazione delle fibre γ. Questa coattivazione dei motoneuroni alfa e gamma fa sì che le fibre intrafusali ed extrafusali si contraggano contemporaneamente. La contrazione simultanea consente di mantenere la reattività dei fusi, impedendo che il fuso sia troppo rilasciato. Secondo alcuni addirittura l'attività gamma può precedere l'attività gamma, funzionando come un meccanismo di servoassitenza, per mantenere il grado di accorciamento indipendentemente dal carico portato.
L'attività dei motoneuroni gamma è controllata
- dalla formazione reticolare, tramite la via reticolo-spinale
- dai nuclei vestibolari, tramite la via vestibolo-spinale
La formazione reticolare eccita spontaneamente i motoneuroni gamma, ma la sua attività viene inibita da impulsi provenienti dalla corteccia motoria, dal cervelletto e dai gangli della base. L'attività gamma viene modulata da una serie di impulsi eccitatori ed inibitori, questi ultimi variabili. In un animale con una sezione fra ponte e mesencefalo (animale decerebrato), gli impulsi inibitori sono eliminati, per cui prevalgono gli impulsi eccitatori. L'animale presenta i muscoli antigravitari irrigiditi (rigidità da decerebrazione), come in una “caricatura della sua normale postura eretta”. Nell'uomo si irrigidiscono tutti i muscoli estensori, anche quelli del braccio (che non sono antigravitari) per la vicinanza filogenetica con gli animali quadrupedi. La decerebrazione è spesso incompatibile con la vita, per cui è più facile riscontrare una rigidità da decorticazione, ottenuta in seguito ad una lesione cerebrale.
Sembra essere basata sul riflesso miotatico anche la reazione positiva di sostegno. È una reazione che si ottiene mettendo a contatto la pianta del piede di un animale spinale con una superficie: i muscoli estensori si contraggono e l'animale può essere messo in piedi, ma non è in grado di mantenere l'equilibrio.
Riflesso inverso da stiramento o miotatico inverso.
Stimolo: tensione muscolare (diversa dalla lunghezza muscolare)
Recettore: organo muscolo-tendineo del Golgi
Via afferente: neurone a T
Centro di integrazione: interneurone e motoneurone α
Via efferente: motoneurone α
Effettore: muscolo da cui è partito lo stimolo
Risposta: rilasciamento
Il significato del riflesso miotatico inverso è quello di impedire che si sviluppi una eccessiva tensione muscolare, che potrebbe danneggiare il muscolo: se poniamo un peso troppo grande sulla mano il bicipite si rilascia ed il peso cade. Il neurone a T, oltre ad attivare i neuroni inibitori dei motoneuroni, stimola anche i motoneuroni eccitatori dei muscoli antagonisti.
L'organo muscolo-tendineo di Golgi è costituito da terminazioni nervose di fibre Ib che si portano su fibre collagene del tendine muscolare. Si tratta quindi di un recettore da stiramento disposto in serie alla fibre muscolari (e non in parallelo, come il fuso neuromuscolare); pertanto è adeguato per rilevare variazioni nella tensione sviluppata dal muscolo.
La funzione dell'organo muscolo tendineo del golgi potrebbe anche essere quella di distribuire la tensione in maniera uniforme su tutto il muscolo: se alcune fibre sono sottoposte ad una tensione maggiore rispetto ad altre, il riflesso da stiramento interverrà in modo da far diminuire la tensione ed uniformarla a quella delle altre fibre.
Riflesso di evitamento (o di allontanamento)
Stimolo: dolore
Recettore: nocicettore cutaneo
Via afferente: via del dolore rapido
Centri di integrazione: neuroni della sostanza grigia
Via efferente: motoneurone α
Effettore: muscolo dell'arto interessato
La funzione del riflesso di allontanamento è quella di allontanare l'arto dallo stimolo nocicettivo.
La contrazione dei muscoli flessori, oltre che alla inibizione dei muscoli antagonisti, è accompagnata da
- contrazione dei muscoli estensori nell'arto controlaterale
- rilasciamento di muscoli flessori dell'arto controlaterale
Tale meccanismo prende il nome di riflesso estensorio crociato e si attiva 0,2-0,5 s dopo il riflesso di allontanamento. Il suo significato funzionale è quello di spostare tutto il corpo lontano dallo stimolo nocivo, oppure di mantenere l'equilibrio (es. uomo che calpesta una puntina: flessione di una gamba, estensione dell'altra).
Riflesso di deambulazione
Un animale spinale, imbragato in modo da avere tutti e quattro gli arti penzolanti, mostra dei movimenti ritmici simil-locomotori, se opportunamente stimolato. Se estendiamo una zampa o se vi poniamo sotto una superficie, la zampa dopo l'iniziale estensione si flette e si porta in avanti; quindi si estende e si porta indietro ed il ciclo si ripete. Per innervazione reciproca, tale riflesso coinvolge gli arti posteriori e l'arto controlaterale. L'arto controlaterale si comporta in maniera opposta; gli arti posteriori sono in fase agli arti anteriori controlaterali.
L'animale spinale, tuttavia, non cammina. È necessario infatti il controllo da parte del tronco encefalico e della corteccia. L'esempio del riflesso di deambulazione è però significativo per dimostrare come talune funzioni del sistema nervoso sono delocalizzate.
Riflessi viscerali
I riflessi viscerali hanno fibre afferenti ed efferenti parasimpatiche. I loro centri di integrazione si trovano a livello del parasimpatico sacrale.
Il riflesso della minzione è stimolato da un aumento della pressione vescicale. Le fibre parasimpatiche stimolano la contrazione della vescia e la minzione. Analogamente, lo sfintere anale, che è tonicamente contratto, si rilascia se il parasimpatico viene stimolato da un'aumentata pressione all'interno del retto. Anche la liberazione di vasodilatanti durante l'eccitamento sessuale è dovuta alla stimolazione di recettori delle fibre afferenti parasimpatiche.
Minzione e defecazione possono essere indotte volontariamente tramite la cotrazione dei muscoli addominali, che aumenta la pressione intraddominale. Anche nell'erezione sono coinvolti i centri soprassiali, per cui l'eccitamento psichico facilita l'insorgere di un'erezione.
Riflessi tronco-encefalici
Riflessi vestibolari
Stimolo: movimento della testa
Recettore: canali semicircolari e macule acustiche dell'utriculo e del sacculo
Via afferente: nervo stato-acustico (VIII)
Centri integratori: nuclei vestibolari
Via efferente: fascio vestibolo-spinale
Effettori: muscoli scheletrici, mm. orbicolari
I riflessi vestibolari tendono a compensare i cambiamenti di posizione della testa. Un animale con sezione fra ponte e mesencefalo reagisce ad un inclinazione in avanti della testa estendendo gli arti anteriori e flettendo i posteriori. Viceversa, se la testa viene spinta all'indietro, l'animale flette gli arti anteriori ed estende quelli posteriori.
Ai riflessi vestibolari è dovuta anche la reazione vestibolare di piazzamento. Un animale in caduta libera si prepara ad atterrare estendendo gli arti. L'estensione è provocata dalla stimolazione dell'utriculo e del sacculo da parte dell'accelerazione del corpo in caduta.
Riflessi cervicali tonici
Stimolo: spostamento del collo
Recettore: fuso neuromuscolare del collo (la regione con più fusi)
Centro di integrazione: formazione reticolare
Via efferente: reticolo-spinale
Effettori: mm. scheletrici
La risposta ai riflessi cervicali tonici è opposta a quella degli stimoli vestibolari. In assenza di stimoli vestibolari, un animale il cui capo venga inclinato in avanti contrae i muscoli posteriori e rilascia i muscoli delle zampe anteriori, come se dovesse guardare all'interno in un buco nel terreno. Viceversa, se la testa dell'animale viene spostata all'indietro, l'animale contrae i muscoli delle zampe anteriori e flette le zampe posteriori, come per guardare sopra un ostacolo. Se all'animale viene girata la testa da un lato, si avrà estensione degli arti appartenenti a quel lato e flessione degli arti controlaterali.
Riflessi di raddrizzamento mesencefalici
tali riflessi tendono a mantenere la testa dritta, la posizione eretta e lo sguardo fisso. Se poniamo un animale mesencefalico esso sarà rigido per la decerebrazione, ma solo se non viene spostato. Se lo teniamo sospeso per il corpo e lo incliniamo da un lato, la sua testa tenderà a mantenersi dritta. Questa risposta prende il nome di riflesso labirintico di raddrizzamento. Se l'animale viene coricato su un fianco, la testa viene mantenuta dritta – anche se i labirinti sono stati distrutti: questo è il riflesso di raddrizzamento della testa evocato dal collo. Se la testa viene raddrizzata da uno dei due meccanismi di cui sopra, l'animale fa dei movimenti per rimettersi in piedi: si tratta del riflesso di raddrizzamento del tronco evocato dal collo. L'animale tende a rimettersi in piedi anche se il raddrizzamento della testa viene impedito: è il riflesso di raddrizzamento del tronco evocato dal tronco, provocato dalla pressione del suolo su un fianco dell'animale.
Se i collegamenti con i centri ottici non sono interrotti, è presente anche un altro riflesso di raddrizzamento, il riflesso visivo di raddrizzamento, che raddrizza l'animale in risposta a stimoli visivi.
Riflesso di prensione
È osservato nei primati a cui sia stato asportato tutto il cervello sopra il talamo. Quando essi giacciono su un fianco, gli arti a contatto con il piano sono in estensione, mentre gli arti del lato opposto sono in flessione. Quando questi vengono stimolati sul palmo tendono ad afferrare qualsiasi oggetto venga a contatto con essi (riflesso di prensione).
Riflessi corticali
Nell'animale decorticato vengono compromessi due riflessi posturali: la reazione di piazzamento e la reazione di sbalzamento. Quest'ultima consiste nei salti laterali che un animale fa – per mantenersi in piedi – quando riceve delle spinte laterali. La reazione di piazzamento si può evocare in un animale bendato: se si porta a contatto con un suo piede un piano, l'animale tende a piazzare saldamente due arti sul piano. Tale reazione si ha anche quando l'animale tocca col naso il piano, o qualora si cerchi di sottrarre un arto al piano su cui era precedentemente appoggiato.
Il sistema motorio dei motoneuroni superiori
Organizzazione sostanza grigia del midollo spinale. I motoneuroni sono organizzati somatotopicamente nel corno ventrale del midollo spinale. Motoneuroni α e γ diretti allo stesso muscolo sono disposti affiancati nella stessa colonna motoneuronale.
Medialmente abbiamo i motoneuroni della muscolatura assiale e prossimale degli arti;
Lateralmente (a livello dei rigonfiamenti cervicale e lombosacrale) abbiamo i motoneuroni della muscolatura distale degli arti.
Gli interneuroni sono organizzati anch'essi in maniera ben precisa:
gli interneuroni mediali proiettano bilateralmente sui motoneuroni mediali;
gli interneuroni laterali proiettano ipsilateralmente sui motoneuroni laterali.
L'organizzazione degli interneuroni riflette l'organizzazione dei movimenti degli arti superiori: i movimenti fini richiedono un controllo indipendente a destra e a sinistra (proiezione ipsilaterale), mentre i movimenti del tronco e dei cingoli richiedono un controllo bilaterale, per il mantenimento della postura.
Classificazione delle vie discendenti motorie: sistemi motori laterale e mediale. Le vie discendenti motorie venivano tradizionalmente divise in vie piramidali ed extrapiramidali. Queste distinzione rifletteva l'osservazione in clinica di malattie piramidali ed extrapiramidali. Tuttavia, in seguito si è visto che non sempre le malattie piramidali sono dovute esclusivamente a perdita di funzione del tratto piramidale; così come le malattie extrapiramidali possono essere dovuta ad alterazioni del fascio corticospinale.
La classificazione odierna divide i sistemi discendenti motori in sistema mediale e sistema laterale, in base alla sede in cui terminano a livello del midollo spinale.
Il sistema mediale termina su motoneuroni ed interneuroni posti medialmente nel corno ventrale, ed è responsabile dei movimenti grossolani del tronco.
Il sistema laterale termina sugli interneuroni della parte laterale del corno ventrale, ed è responsabile dei movimenti fini degli arti.
Sistema motorio laterale – fascio cortico-spinale laterale
Il fascio cortico-spinale origina a livello delle aree motoria, premotoria e motoria supplementare. Le cellule da cui originano sono cellule piramidali di grandi e piccole dimensioni del V strato corticale e cellule gigantopiramidali di Betz.
A livello del bulbo, circa l'80% delle fibre decussa e si porta nel funicolo dorsolaterale per formare il fascio-corticospinale laterale. La parte che non decussa prosegue nel cordone anteriore e forma il fascio cortico-spinale ventrale.
La corteccia motoria ha un'organizzazione topografica molto simile a quella della corteccia somatosensoriale, per cui è possibile disegnare un homunculus motorio in rapporto ad una sezione coronale della corteccia. Anche in questo caso le proporzioni delle parti del corpo non sono rispettate, poiché non c'è corrispondenza fra dimensione reale della zona corporea e grandezza della regione corticale deputata la suo controllo. Le parti più grandi dell'homunculus sono le mani e la faccia, evidentemente quelle che richiedono un movimento più controllato. La costruzione della mappa somatotopica della corteccia motoria è stata fatta mediante esperimenti di elettrostimolazione. La stimolazione di una determinata zona corticale, determina infatti contrazioni di una parte del corpo ben precisa.
Sistema motorio laterale – fascio rubrospinale
La sua appartenenza al sistema motorio laterale è ancora discussa. Origina a livello della porzione magnocellulare del nucleo rosso mesencefalico, che a sua volta riceve afferenze dalla corteccia motoria e dal cervelletto (nuclei globoso ed emboliforme). Decussa a livello della porzione inferiore del tronco encefalico e si porta sugli interneuroni e motoneuroni che controllano i muscoli distali degli arti.
Fascio cortico-bulbare
Questo fascio ha la stessa origine del fascio corticospinale ed appartiene in parte al sistema laterale, in parte al sistema mediale. Dopo la sua origine a livello corticale, le fibre del fascio corticobulbare si portano nel tronco encefalico, dove
- in parte si portano ai nuclei controlaterali dei nervi faciale (VII) e ipoglosso (XII), costituendo così un fascio che ha le stesse funzioni per il capo del fascio corticospinale laterale (movimenti fini: movimenti mimici e movimenti della lingua per fonazione e deglutizione)
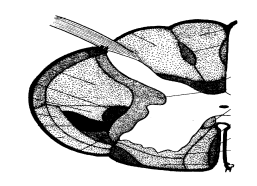 in parte termina bilateralmente, costituendo così un fascio analogo al fascio corticospinale ventrale (movimenti grossolani: muscoli orbicolari)
in parte termina bilateralmente, costituendo così un fascio analogo al fascio corticospinale ventrale (movimenti grossolani: muscoli orbicolari)
Sistema motorio mediale – fascio corticospinale ventrale
Origina anch'esso dalle aree motoria, premotoria e motoria supplementare. Le sue fibre non decussano a livello del bulbo, ma a livello spinale, dove attraversano la commessura bianca e si portano bilateralmente su interneuroni che proiettano bilateralmente sui motoneuroni mediali del corno ventrale. La funzione di questo fascio, come detto, è quella di sovrintendere a movimenti grossolani, per il mantenimento dell'equilibrio.
 Sistema motorio mediale – fascio vestibolo-spinale
Sistema motorio mediale – fascio vestibolo-spinale
Origina a livello dei nuclei vestibolari (mediale e laterale) e termina bilateralmente sui motoneuroni mediali. I nuclei vestibolari ricevono afferenze dai canali semicircolari e dalle macule, che portano informazioni su accelerazione rotatoria e lineare e posizione della testa.
La funzione del fascio è quella di provvedere ad aggiustamenti posturali in seguito ai movimenti della testa.
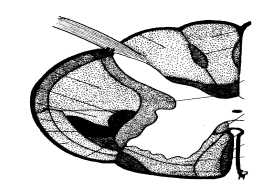
Sistema motorio mediale – fascio reticolo-spinale
Esistono due fasci reticolo-spinali, uno pontino ed uno bulbare. Il primo origina a livello della formazione reticolare pontina e discende nel cordone anteriore ispilaterale. Termina sugli interneuroni del gruppo mediale. La sua funzione è quella di attivare i motoneuroni che innervano i muscoli estensori prossimali, per il mantenimento della postura.
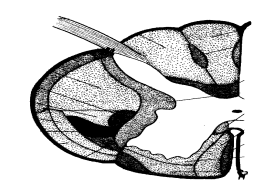 Il fascio reticolospinale che origina a livello del bulbo decorre nel cordone laterale e proietta bilateralmente con giunzioni inibitorie.
Il fascio reticolospinale che origina a livello del bulbo decorre nel cordone laterale e proietta bilateralmente con giunzioni inibitorie.
Sistema motorio mediale – fascio tettospinale
origina da neuroni localizzati negli strati profondi del collicolo superiore. Decussa a livello della formazione grigia periacquedutturale e decorre nel cordone anteriore. Termina sui motoneuroni mediali dei segmenti cervicali.
La sua funzione è quella di produrre movimenti del capo in seguito a stimoli visivi, uditivi e somatici.
Vie dirette ed indirette dalla corteccia al midollo spinale.
- dirette: fascio cortico-spinale e cortico-bulbare
- indirette: fascio cortico-rubro-spinale e cortico-reticolo-spinale
Sommario delle vie di controllo dei motoneuroni inferiori
sistema laterale (controllo parti distali – movimenti fini)
- via cortico-spiale laterale
- via cortico-bulbare
- via rubro-spinale
sistema mediale (controllo parti assiali – movimenti grossolani)
- via cortico-spinale ventrale
- via cortico-bulbare
 via vestibolo-spinale (mediale e laterale)
via vestibolo-spinale (mediale e laterale)- via reticolo-spinale (bulbare e pontina) origine a livello del tronco encefalico
- via tetto-spinale
Generalità sul movimento volontario. I movimenti riflessi sono atti motori semplici e stereotipati, evocati in risposta stimoli specifici. I movimenti volontari rispondono ad uno stesso stimolo in maniera diversa a seconda dell'obbiettivo; mostrano apprendimento; possono essere generati da istruzioni interne. Queste caratteristiche distinguono i movimenti volontari dai movimenti riflessi. Negli animali superiori i centri superiori sono in grado di dissociare nello stimolo le informazioni e la capacità di indurre movimento.
Fasi fondamentali nel movimento volontario. Il primo stadio nella generazione di un comando motorio è l'identificazione della finalità del movimento, che viene ottenuta in gran parte in base alla convergenza delle informazioni sensoriali. Questa prima tappa avviene nella corteccia parietale posteriore (area di associazione posteriore). L'origine dei comandi motori può provenire anche dall'area di associazione anteriore. Le informazioni vengono quindi trasmesse all'area supplementare motoria, dove viene elaborato un “programma motorio”: quali muscoli contrarre, in che sequenza e per quanto tempo per ottenere il movimento desiderato. Il programma motorio viene eseguito dalla corteccia motoria primaria, che lo invia ai motoneuroni spinali tramite i fasci cortico-spinale e corticobulbare e le altre vien indirette (cortico-rubro-spinale, cortico-reticolo-spinale). Vengono così reclutate le diverse unità motorie, i muscoli si contraggono e si ha il movimento.
Il movimento stesso produce delle informazioni somatosensioriali fondamentali per la correzione a feedback del movimento stesso. Le informazioni sensitive vengono inviate alla corteccia sensitiva, che le invia a sua volta al cervelletto, che valuta la correttezza del movimento in base al programma motorio. Da qui le informazioni vengono trasmesse alla corteccia motoria, per l'eventuale correzione. Oltre al cervelletto, è attivo un altro sistema di controllo, quello dei gangli della base.
Aree associative. Nell'uomo sono particolarmente sviluppate le aree associative, aree cerebrali superiori che associano l'ingresso sensoriale all'uscita motoria. Nelle aree associative si compiono tutti i processi mentali coinvolti fra la sensazione ed il movimento.
- area associativa posteriore. Si trova al confine tra i lobi parietale, occipitale e temporale. Collega informazioni provenienti da modalità sensoriali diverse, come la percezione (riconoscere una chiave al tatto) ed il linguaggio (contiene l'area di Wernicke)
- area associativa limbica. Si trova nel margine mediale degli emisferi cerebrali. È responsabile del comportamento emotivo e della conservazione delle tracce mnemoniche
- area associativa anteriore. È contenuta nella corteccia prefrontale. È responsabile della pianificazione del movimento.
Schema generale del controllo motorio
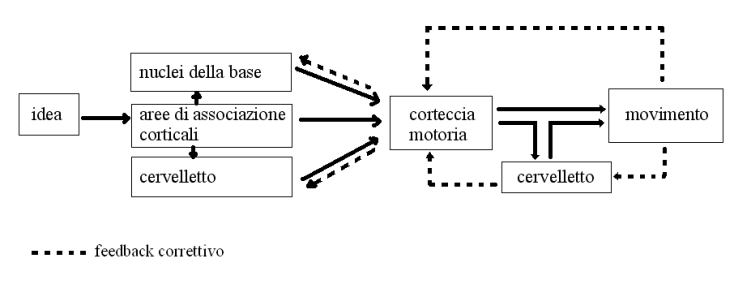 Ruolo della corteccia motoria
Ruolo della corteccia motoria
La corteccia motoria programma il movimento assieme ai nuclei della base ed al cervelletto. Successivamente la corteccia motoria invia il programma motorio verso il basso, al midollo spinale ed al tronco encefalico; un copia del programma motorio viene inviata anche al cervelletto in modo che conosca il programma inviato ai motoneuroni α.
Afferenze
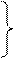 c. somatosensitiva primaria
c. somatosensitiva primaria
area associativa posteriore corteccia motoria primaria
gangli della base e cervelletto
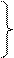 area associativa anteriore
area associativa anteriore
area associativa posteriore corteccia premotoria
gangli della base e cervelletto
Il sottosistema motorio del cervelletto
Caratteristiche comuni dei gangli della base e del cervelletto
Sia il cervelletto che i gangli della base hanno uno schema di connessioni organizzato in:
- regione centrale di elaborazione
- nuclei intermedi di trasmissione
- talamo
- ritorno ad 1.
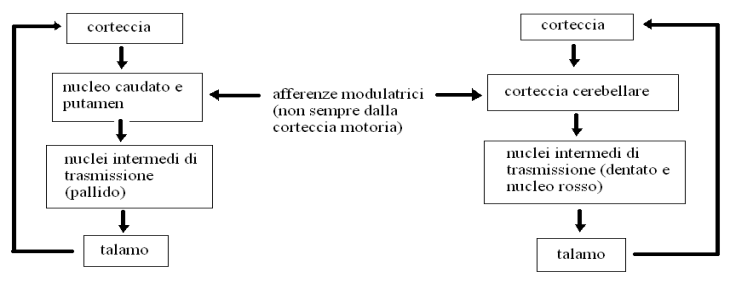
Cervelletto e gangli della base hanno però un ruolo nella motilità diverso:
gangli della base
- lavorano (anche) nella fase preparatoria del movimento
- pianificazione, avvio e completamento movimenti
- movimenti con componenti cognitive e complesse
cervelletto
- controllo movimenti in atto
Organizzazione anatomo-funzionale del cervelletto. Il cervelletto è una formazione emisferica, che occupa la fossa cranica posteriore, al di sotto del lobo occipitale, dal quale è separato dal tentorio del cervelletto. Anatomicamente è costituito da tre lobi: anteriore, posteriore e flocculonodulare, separati fra loro dalla scissura primaria e dalla scissura posterolaterale. Considerando la sezione sagittale, il cervelletto può essere diviso in: emisferi, verme e tonsille.
Lo strato superficiale è costituito da una corteccia simile a quella cerebrale; all'interno del cervelletto troviamo la sostanza bianca, in analogia con il cervello. All'interno della sostanza bianca cerebellare si trovano i nuclei cerebellari profondi, che sono i nuclei dentato, globoso ed emboliforme e il nucleo del tetto. Le afferenze cerebellari giungono sia alla corteccia che ai nuclei profondi, mentre le efferenze partono solo dai nuclei profondi.
Sulla base del profilo filogenetico, il cervelletto viene suddiviso in:
- archicerebellum, è la regione che corrisponde al lobulo flocculo-nodulare. Contiene il nucleo del fastigio (o del tetto) ed è dominato dalle afferenze vestibolari, per cui è anche chiamato vestibolocervelletto;
- paleocerebellum, corrisponde anatomicamente al lobo anteriore, al verme ed alle tonsille. Contiene anch'esso il nucleo del fastigio ed i nuclei interpositi (globoso ed emboliforme). È dominato dalle afferenze spinali, da cui il nome di spinocervelletto;
- neocerebellum, corrisponde alla regione degli emisferi. Contiene il nucleo dentato ed è dominato dalle afferenze corticali, per cui viene chiamato anche corticocervelletto.
La faccia anteriore del cervelletto è connessa al tronco encefalico grazie a tre peduncoli:
- il peduncolo superiore contiene fibre efferenti dai nuclei profondi del cervelletto al nucleo rosso, al collicolo superiore e alle aree motorie priamria e secondaria
- il peduncolo medio contiene fibre afferenti dai nuclei basilari del ponte e da molte aree corticali
- il peduncolo inferiore contiene afferenze dai nulcei vestibolari e i fasci spinocerebellari; efferenze ai nuclei vestibolari e alla formazione reticolare.
La corteccia cerebellare è organizzata in tre strati:
- strato molecolare, esterno. Contiene gli alberi dendritici delle cellule di Purkinje e gli assoni delle cellule dei granuli, organizzati in strutture perpendicolari fra loro. Sui dendriti delle cellule di Purkinje terminano le fibre rampicanti ad aspartato.
- strato delle cellule di Purkinje, intermedio, ha lo spessore di una sola cellula. Gli assoni delle cellule di Purkinje costituiscono l'unica efferenza della corteccia cerebellare e sono dirette ai nuclei profondi.
- strato granulare, costituito dalle cellule dei granuli. Qui terminano le fibre muscoidi ad acetilcolina.
Vestibolo-cervelletto
afferenze vie vestibolari dirette ed indirette (prevalentemente dal nucleo inferiore)
informazioni visive dai collicoli superiori del mesencefalo
efferenze formazione reticolare
funzione mantenimento dell'equilibrio statico e dinamico
controlla il movimento coordinato di capo ed occhi
lesioni alterazioni dell'equilibrio: il soggetto cammina su base allargata
Spino-cervelletto
afferenze corteccia motoria: porta il programma motorio
nucleo rosso
nucleo vestibolare
collicolo superiore: informazioni visive
vie spinocerebellari (dorsale e ventrale)
fascio cuneocerebellare (impulsi propriocettivi da testa e collo)
collaterali della via spino-bulbo-talamo-corticale
efferenze porzione magnocellulare nucleo rosso ----> fascio rubrospinale
talamo (VL)----> corteccia motoria
funzione confronta il programma motorio (copia teorica) con le afferenze somatiche (copia pratica);
regola la postura durante i movimenti volontari
apprendimento motorio
lesioni i nuclei dello spinocervelletto sono tonicamente attivi; una loro lesione porta ad una diminuita eccitabilità dei neuroni;
difficoltà nel correggere i movimenti: dismetria (errori di dimensione ed ampiezza), atassia (scarsa coordinazione), tremore intenzionale (manca lo smorzamento di un movimento e deve intervenire un meccanismo a feedback)
Cortico-cervelletto
afferenze esclusivamente dalla corteccia, mediate dai nuclei basilari del ponte:
aree motoria e premotoria, somatosensitiva I e II, aree associative visiva e posteriore
efferenze nucleo rosso---> talamo (VL) ---> corteccia motoria
nucleo rosso---> oliva inferiore ---> cervelletto (circuito a feedback)
funzione pianificazione: consente di passare ordinatamente da un movimento a un altro
temporizzazione: consente di prevedere di quanto si muoveranno in un certo tempo le diverse parti del corpo; consente di passare da un movimento ad un altro
lesioni coinvolgono i movimenti distali e di prensione: ritardi nell'inizio del movimento, irregolarità nella sequenza temporale, decomposizione del movimento, difficoltà a muovere indipendentemente le dita, il soggetto riferisce che deve pensare ad ogni movimento, non riesce a compiere la pronosupinazione della mano
Il sottosistema motorio dei gangli della base
i gangli della base sono i nuclei profondi del cervello e contribuiscono, assieme al cervelletto, alla regolazione dell'attività motoria. Con il termine gangli della base si indicano in genere cinque strutture:
- il nucleo caudato
- il putamen
- il globo pallido (diviso in un segmento interno ed uno esterno)
- il nucleo subtalamico
- la sostanza nera (diviso in parte compatta e parte reticolare)
Putamen e globo pallido formano il nucleo lenticolare.
Caudato e putamen formano lo striato; con l'aggiunta del globo pallido formano il corpo striato.
Le funzioni dei nuclei della base non sono ancora del tutto chiare. I nuclei della base influenzano la motilità agendo sui motoneuroni superiori. Essi infatti non proiettano direttamente ai motoneuroni inferiori, ma formano un circuito che unisce la maggior parte delle aree corticali con la corteccia motoria.
I gangli della base controllano i movimenti che richiedono una certa destrezza durante la lro esecuzione; sono coinvolti nei processi cognitivi motori e regolano ampiezza e velocità dei movimenti.
Le principali afferenze dei nuclei della base giungono allo striato da:
- corteccia cerebrale (quasi tutte le aree corticali: aree associative anteriore e posteriore, lobo temporale, insula, circonvoluzione del cingolo)
- talamo
- tronco encefalico
Le fibre afferenti utilizzano il glutammato come neurotrasmettitore ed hanno un'elevata attività tonica.
Le principali efferenze vanno dal globo pallido interno e dalla parte reticolata della sostanza nera a:
- talamo ---> da qui alla corteccia motoria (premotoria e motoria primaria) e all'area associativa anteriore
- tronco encefalico
Si tratta di fibre inibitorie, che utilizzano il GABA. La loro scarica è tonica, cosicché il talamo è tonicamente inibito: la corteccia cerebrale, a sua volta, è inibita.
Circuiti dei gangli della base: via diretta
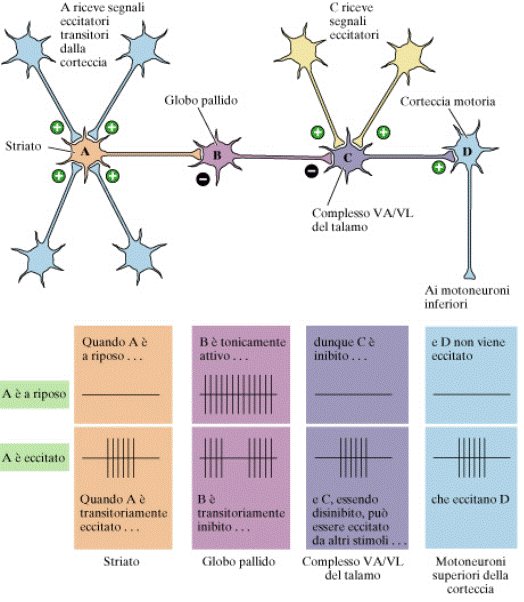 La via diretta disinibisce il talamo. La parte compatta della sostanza nera va ad eccitare lo striato. L'attività tonica dello striato è quella di inibire il globo pallido mediale. Nei periodi in cui il globo pallido viene inibito, esso non può esercitare la sua inibizione sul talamo (“inibizione dell'inibizione”). Il talamo a sua volta, può attivare transitoriamente la corteccia motoria: il movimento viene facilitato.
La via diretta disinibisce il talamo. La parte compatta della sostanza nera va ad eccitare lo striato. L'attività tonica dello striato è quella di inibire il globo pallido mediale. Nei periodi in cui il globo pallido viene inibito, esso non può esercitare la sua inibizione sul talamo (“inibizione dell'inibizione”). Il talamo a sua volta, può attivare transitoriamente la corteccia motoria: il movimento viene facilitato.
Circuiti dei gangli della base: via indiretta
Utilizzando la via indiretta, la parte compatta della sostanza nera va ad inibire transitoriamente i recettori D2 dello striato. Lo striato va ad inibire transitoriamente il segmento esterno del globo pallido, che tonicamente inibisce il nucleo subtalamco. Anche qui si ha un'inibizione dell'inibizione, il cui risultato è un'attivazione transitoria del globo pallido interno. Quest'ultimo è già di per sé tonicamente attivo (inibisce il talamo) ed una sua ulteriore attivazione non fa altro che aumentare l'inibizione talamica. Il talamo non può attivare la corteccia e il movimento viene inibito.
Sintomi da lesioni dei gangli della base
La via indiretta modula gli effetti di disinibizione della via diretta: si crea normalmente un equilibrio dinamico, sia a riposo che in movimento, tra gli effetti delle due vie. In caso di patologie il complesso equilibrio tra via diretta ed indiretta si può alterare. Tre tipi di sintomi insorgono:
1. tremori e movimenti involontari
tremore a riposo
corea: movimenti rapidi involontari di “danza”
atetosi: lenti movimenti di contorsione
ballismo: rapide proiezioni degli arti
2. alterazioni della postura e del tono muscolare
rigidità, atteggiamento in flessione
3. repertorio motorio ridotto e lentezza dei movimenti, ma non paralisi
diminuzione movimenti associati (oscillamento braccia)
difficoltà ad iniziare un movimento ed a terminarlo
Morbo di Parkinson: sintomi ed alterazioni dei circuiti
Il morbo di parkinson è dovuto alla perdita di neuroni dopaminergici della sostanza nera che proiettano allo striato (fibre nigrostriatali). I sintomi sono sia ipercinetici sia ipocinetici (dominanti):
- tremore riposo, scompare con il movimento
- rigiditá dei muscoli degli arti (a tubo di piombo)
- difficoltá ad iniziare i movimenti ed a terminarli
- diminuzione movimenti spontanei
- lentezza nell’esecuzione di movimenti complessi (bradicinesia)
- andatura rallentata e strascicata, lentezza nel parlare
- alterazione mimica facciale

L'alterazione dei circuiti è la seguente: la via diretta degenera, per cui la sostanza nera non va più ad eccitare come prima lo striato. Questo a sua volta non inibisce il pallido interno, che quindi è libero di inibire tonicamente il talamo, con conseguente inibizione del movimento.
Anche la via indiretta degenera: la sostanza nera non va ad inibire lo striato, che è libero di inibire il pallido esterno. Il pallido esterno non può inibire il nucleo subtalamico, che attiva fortemente il pallido esterno, con conseguente inibizione del talamo. Anche in questo caso il movimento viene inibito.
Il trattamento del morbo di Parkinson viene effettuato con L-dopa e L-deprenil. Quest'ultimo è un inibitore del monoamino-ossidasi, gli enzimi responsabili della distruzione della dopamina dopo che queste è stata secreta. Una soluzione chirurgica era quella di eliminare i collegamenti fra i nuclei della base ed il talamo. Questo metodo – risultato molto efficace in esperimenti sulle scimmie – poteva portare a seri deficit neurologici.
Corea di Huntington: sintomi ed alterazione dei circuiti
La corea è una malattia autosomica dominante, dovuta ad una degenerazione bilaterale dei neuroni GABAergici del nucleo caudato. I sintomi consistono in una serie di movimenti incontrollati (corea: danza), rapidi improvvisi, irregolari e a scatti. La demenza è un sintomo dell malattia allo stato avanzato.
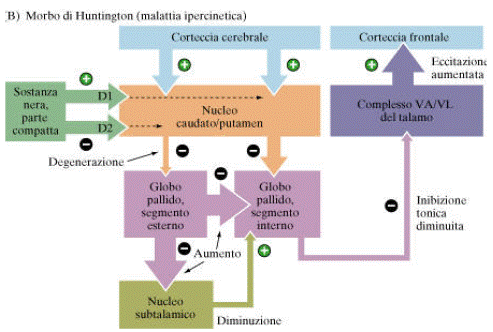
L'alterazione dei circuiti è la seguente. A livello della via indiretta diminuiscono le fibre che inibiscono il pallido esterno. Il pallido esterno così inibisce in maniera continua il nucleo subtalamico, che non va ad attivare il pallido interno. L'attività tonica del pallido risulta diminuita: diminuisce l'inibizione del talamo e la corteccia motoria viene eccitata maggiormente.
Il sistema nervoso autonomo
Sezioni:simpatico, parasimpatico, enterico
Il sistema nervoso simpatico può essere considerato come una parte del sistema nervoso motorio nella quale le strutture effettrici sono, invece dei muscoli scheletrici, la muscolatura liscia, la muscolatura cardiaca e le ghiandole. Il sistema nervoso autonomo viene diviso in sistema nervoso parasimpatico ed ortosimpatico.
Il sistema parasimpatico controlla la routine e l'attività tranquilla del vivere quotidiano: favorisce la digestione, stimolando la motilità gastrica e rilasciando il piloro; il diametro pupillare si riduce, la frequenza cardiaca si abbassa e si ha vasodilatazione. Per questo motivo viene definito in inglese sistema “rest and digest”, cioè sistema riposa e metabolizza. Contemporaneamente all'attivazione del parasimpatico si ha una diminuzione dell'attività simpatica.
Il sistema ortosimpatico domina nelle situazioni da stress: viene infatti chiamato sistema “fight or flight” (lotta o fuggi) in quanto prepara l'organismo ad affrontare una situazione pericolosa o – eventualmente – a fuggire. Una scarica massiva e simultanea del simpatico produce numerose risposte:
- le pupille si dilatano, le palpebre si ritirano: più luce alla retina e facilitazione movimenti oculari
- vasocostrizione a livello della pelle e dell'intestino: il sangue viene dirottato ai muscoli
- broncodilatazione: facilitazione dell'ossigenazione del sangue
- brachicardia e aumento forza di contrazione cardiaca: aumento perfusione di muscoli e cervello
- liberazione adrenalina e noradrenalina: aumento pressione arteriosa
- inibizione peristalsi intestinale
- favorisce il metabolismo dei glucidi
- piloerezione
In realtà non sempre si ha una scarica simpatica così massiccia, ma il controllo simpatico e parasimpatico agiscono insieme per il mantenimento dell'omeostasi. Il controllo delle attività corporee può così oscillar da un sistema all'altro.
Simpatico e parasimpatico assieme soddisfano tutte le proprietà dell'omoeostasi di Cannon:
- mantengono la costanza del mezzo interno
- hanno un livello tonico di attività che può essere modificato (per es. per il calibro vasale)
- esercitano un controllo antagonista (ma non sempre)
- danno risposte tissutali diverse a seconda del diverso recettore di membrana
Il controllo antagonista viene esercitato sulla maggior parte degli organi (occhio, cuore, polmoni, stomaco, intestino, vescica). Su alcuni organi invece non è possibile un controllo antagonista. Le ghiandole sudoripare, la midollare del surrene e i muscoli erettori dei peli non hanno un'innervazione simpatica, per cui il loro controllo viene effettuato esclusivamente dal simpatico tramite un aumento o una diminuzione della propria attività. Talvolta simpatico e parasimpatico possono avere un controllo sinergico su un organo effettore: è il caso degli organi genitali maschili, in cui il parasimpatico sostiene l'erezione e il simpatico è responsabile dell'eiaculazione.
Un esempio di diversa risposta a seconda del recettore è quello classico dell'adrenalina: i recettori α danno vasocostrizione, mentre i recettori β danno vasodialtazione. La noradrenalina, invece, è sempre vasocostrittrice.
Organizzazione generale del sistema autonomo. Il sistema nervoso simpatico e quello parasimpatico sono costituiti da due tipi di neuroni:
- i neuroni pregangliari, i cui corpi sono situati nel SNC;
- i neuroni postgangliari, i cui corpi sono situati in uno dei gangli autonomi.
 Organizzazione sistema ortosimpatico. I neuroni pregangliari del sistema ortosimpatico sono situati nella colonna intermediolaterale (o corno laterale) della sostanza grigia del midollo spinale, a livello di T1-L3. Sono concettualmente paragonabili agli interneuroni del sistema motorio somatico, poiché non innervano il tessuto effettore. I loro assoni, piccoli e mielinici, escono attraverso la radici ventrali dei nervi spinali. Si portano attraverso il ramo comunicante bianco nel ganglio paravertebrale situato alla stessa altezza da cui sono usciti.
Organizzazione sistema ortosimpatico. I neuroni pregangliari del sistema ortosimpatico sono situati nella colonna intermediolaterale (o corno laterale) della sostanza grigia del midollo spinale, a livello di T1-L3. Sono concettualmente paragonabili agli interneuroni del sistema motorio somatico, poiché non innervano il tessuto effettore. I loro assoni, piccoli e mielinici, escono attraverso la radici ventrali dei nervi spinali. Si portano attraverso il ramo comunicante bianco nel ganglio paravertebrale situato alla stessa altezza da cui sono usciti.
A questo punto l'assone del neurone pregangliare ha due possibilità:
- contrae sinapsi a livello del ganglio paravertebrale. Da qui l'assone del neurone postgangliare, amielinico, si porta attraverso il ramo comunicante grigio all'interno del nervo spinale. La componente simpatica nei nervi spinali rappresenta circa l'8% delle fibre.
È il comportamento della parte alta del midollo spinale. Queste fibre nervose innervano il cuore, i polmoni, le ghiandole salivari, le strutture effettrici della pelle.
- Passa del ganglio paravertebrale senza fare sinapsi ed esce formando i nervi splancnici. Arriva ai gangli prevertebrali e fa sinapsi con i neuroni post-gangliari. Alcuni assoni pregangliari possono superare anche il ganglio prevertebrale e portarsi in gangli più periferici, o addirittura arrivare all'organo da innervare (è il caso della midollare del surrene). Queste fibre nervose, che si trovano più in basso rispetto alle precedenti, innervano stomaco, pancreas, fegato, midollare surrenale, intestino, vescica, apparato genitale.
I gangli prevertebrali sono:
- cervicale superiore (C1-C4)
- cervicale medio (C5-C6)
- ganglio stellato (C7-T1)
- ganglio celiaco
- ganglio mesenterico superiore ed inferiore
- ganglio ipogastrico
Organizzazione del sistema parasimpatico. Il sistema parasimpatico cervicale ha i propri neuroni pregangliari a livello dei nuclei parasimpatici del tronco encefalico. I neuroni postgangliari sono situati a livello dei gangli cervicali. I nuclei visceromotori del tronco encefalico sono:
- nucleo di Edinger-Westphal (III, mesencefalo): i neuroni postgangliari si trovano a livello del ganglio ciliare e controllano i muscoli ciliare e sfintere della pupilla;
- ganglio muco-naso-lacrimale (VII, ponte): i neuroni postgangliari si trovano nel ganglio sfenopalatino ed innervano le ghiandole delle mucose nasale e palatina e la ghiandola lacrimale;
- nucleo salivatorio superiore (VII, ponte): i neuroni postgangliari si trovano nei gangli sottomadibolare e sottolinguale e innervano le ghiandole omonime;
- nucleo salivatorio inferiore (IX, bulbo): i neuroni postgangliari si trovano nel ganglio otico e innervano la ghiandola parotide;
- nucleo motore dorsale (X, bulbo): i neuroni postgangliari si trovano in gangli prossimi al cuore, ai polmoni ed all'apparato digerente, che innervano.
Il sistema parasimpatico ha i suoi neuroni pregangliari all'interno della colonna intermediolaterale del tratto sacrale (S2-S4). I loro assoni si uniscono a formare i nervi pelvici, che si portano ai gangli parasimpatici, dove contraggono sinapsi con fibre postgangliari. I gangli parasimpatici sono piccoli e numerosi e sono situati in prossimità degli organi che innervano (vescica, colon, retto, organi genitali).
Sistema nervoso enterico. Molti neuroni controllano le funzioni del tratto gastrointestinale: è stato calcolato che sono coinvolti neuroni in numero uguale (o maggiore) che nel midollo spinale. Oltre al controllo parasimpatico ed ortosimpatico, vi è un esteso sistema di cellule che non è riconducibile a nessuno dei due: tale sistema viene definito sistema nervoso enterico ed è il responsabile di numerose funzioni viscerali che continuano a manifestarsi anche in assenza di innervazione simpatica.
Il sistema enterico è costituito
- dal plesso mioenterico di Auerbach, situato fra strato esterno ed interno della muscolatura esterna del tratto gastrointestinale. Il suo ruolo è quello di coordinare la motilità del tratto gastrointestinale;
- dal plesso sottomucoso di Meissner, che si trova al di sotto dello strato mucoso. La sua funzione è quella di regolare il trasporto di acqua e di ioni attraverso l'epitelio intestinale e le secrezioni ghiandolari.
I due plessi sono costituiti da tre tipi di neuroni: i neuroni sensitivi, che verificano le condizioni meccaniche della parete e il contenuto del tratto, interneuroni, che integrano le informazioni, motoneuroni, che controllano il muscolo liscio e le ghiandole. Tale costituzione ricorda quella degli archi riflessi ed in parte il sistema enterico lavora come un arco riflesso. Non bisogna dimenticare, però, che l'attività del sistema enterico viene modulata dal sistema simpatico. Questo infatti può inibire la motilità tramite il rilascio di adrenalina, può ridurre l'afflusso sanguigno tramite il rilascio di adrenalina e neuropeptide Y e può regolare anche l'attività delle ghiandole gastrointestinali. Un corretto funzionamento del tratto gastrointestinale richiede anche il controllo da parte del sistema nervoso centrale.
Componenti sensoriali del sistema autonomo. I neuroni sensitivi del sistema enterico sono neuroni pseudounipolari a T contenuti nelle radici dorsali dei nervi spinali. A livello del parasimpatico cervicale i neuroni sensitivi si trovano nei gangli genicolato, petroso e nodoso (VII, IX e X). Il ramo centrifugo è in contatto con il recettore.
Il ramo centripeto si porta in prossimità del corno laterale, per i riflessi locali, oppure al nucleo del tratto solitario. Il nucleo del tratto solitario proietta all'ipotalamo e al tegmento del tronco encefalico. Questo circuito è fondamentale per le funzioni riflesse automatiche (controllo cardiovascolare, della vescica, dell'apparato riproduttivo, dell'apparato respiratorio...)
Controllo centrale funzioni motorie viscerali
Neurotrasmettitori e recettori. Il neurotrasmettitore utilizzato nelle sinapsi tra i neuroni pregangliari ed i neuroni postgangliari è l'acetilcolina. Nei gangli del sistema nervoso autonomo esistono due tipi di recettori:
- recettori nicotinici (così chiamati per la loro risposta alla nicotina). Sono canali ligando-dipendenti eccitatori, che fanno entrare ioni postivi. Mediano risposte rapide. Sono bloccati dal curaro.
- recettori muscarinici (così chiamati per la loro risposta alla muscarina). Sono dei recettori metabotropi associati alle proteine G, che provocano la chiusura dei canali del K. Inibiscono così la corrente M, dovuta ad un aumento di conduttanza del potassio, con conseguente aumento dell'eccitazione e prolungamento del PPSE. Mediano risposte lente e sono bloccati dall'atropina.
I neurotrasmettitori utilizzati dai neuroni postgangliari sono diversi tra sistema simpatico e parasimpatico.
Il parasimpatico utilizza ancora l'acetilcolina, con tre tipi di recettori muscarinici, M1, M2, M3. Sono recettori a serpentina, accoppiati tramite proteine G a canali per il K, fosfolipasi C e adenil-ciclasi.
Il simpatico utilizza la noradrenalina, che ha quattro tipi di recettori, tutti accoppiati a proteine G:
- α1: attiva la fosfolipasi C--> IP3 --> aumento Ca intracellulare, più sensibile a NA
- α2: riduzione dell'AMPc mediata dalla proteina G, più sensibile a NA
- β1 (sensibile in egual modo a noradrenalina e adrenalina)
- β2 (più sensibile all'adrenalina)
I recettori alfa e beta hanno effetti opposti: α1 stimolato da NA provoca contrazione del muscolo liscio dei vasi, β2 stimolato da A provoca vasodilatazione.
Oltre alla noradrenalina, il simpatico utilizza anche l'acetilcolina a livello delle ghiandole sudoripare.
Effetti della scarica simpatica e parasimpatica a livello degli organi viscerali
organo effettore |
parasimpatico |
simpatico |
occhio |
Miosi, contrazione m. ciliare |
Midriasi,rilasciamento m.ciliare |
cuore |
Diminuzione frequenza, contrattilità e velocità di conduzione |
Aumento frequenza, contrattilità e velocità di conduzione |
arterie |
Vasodilatazione (vasocostrizione delle coronarie) |
α: vasocostrizione |
polmoni muscoli bronchiali |
contrazione |
rilasciamento |
ghiandole bronchiali |
stimolazione |
α1: inibizione |
stomaco e intestino sfinteri |
rilasciamento |
contrazione |
tono e motilità |
aumento |
diminuzione |
secrezione |
stimolazione |
inibizione |
vescica detrusore |
contrazione |
rilasciamento |
sfintere e trigono |
rilasciamento |
contrazione |
ureteri |
aumento tono |
aumento tono |
utero |
variabile |
α1: contrazione (se gravido) |
pene |
erezione |
eiaculazione |
midollare surrene |
--- |
secrezione di adrenalina e noradrenalina |
fegato |
--- |
glicogenolisi |
pancreas (acini e isolotti) |
aumentata secrezione |
α: diminuita secrezione |
ghiandole salivari |
secrezione profusa, acquosa |
secrezione densa, vischiosa |
tessuto adiposo |
--- |
lipolisi |
Ruolo del tronco encefalico, dell'ipotalamo e della corteccia
I livelli di integrazione autonomica sono disposti – come i corrispondenti livelli di integrazione somatica, in scala gerarchica.
I riflessi semplici, quali lo svuotamento della vescica piena, sono integrati a livello spinale.
Nel bulbo sono integrati riflessi che regolano il respiro e la pressione sanguigna, la deglutizione, la tosse, lo starnuto ed il vomito.
Nel mesencefalo sono integrati i riflessi che controllano le risposte pupillari alla luce.
Nell'ipotalamo sono integrati i processi che mantengono la costanza chimica e termica dell'ambiente interno.
La corteccia cerebrale media risposte viscerali con componenti emotive e legate all'esperienza (arrossire, pallore da paura, reazioni autonome del comportamento sessuale)
schema di controllo centrale delle funzioni viscerali (?)
Ipotalamo. L'ipotalamo è la parte del diencefalo che si trova al di sotto del solco ipotalamico. In esso distinguiamo parecchi nuclei. I nuclei ipotalamici più importanti, in direzione rostrocaudale, sono: preottici, sovrachiasmatico, sovraottici, paraventricolare, arcuato, ventromediale, dorsomediale, mammillari.
Le principali funzioni dell'ipotalamo sono:
- attivazione del SN simpatico
- controlla il rilascio delle catecolamine nella midollare del surrene
- contribuisce al mantenimento della glicemia agendo sul pancreas endocrino
- regolazione delle temperatura corporea
- controllo dell'osmolarità corporea
- sete
- secrezione di ADH
- controllo assunzione di cibo
- centro della fame
- centro della sazietà
- controllo delle funzioni riproduttive
- secrezione di ossitocina
- liberazione di RF per FSH e LH
- interagisce con il sistema limbico per controllare il comportamento e le emozioni
- contribuisce a regolare il ciclo sonno-veglia
- influenza il centro di controllo cardiovascolare del bulbo
- controlla l'attività dell'ipofisi anteriore mediante RF/IF
Termoregolazione
Gli animali omeotermi hanno una temperatura ottimale per le loro funzioni corporee. I valori normali per l'uomo sono compresi fra i 36,3 e 37,1 °C. la temperatura è diversa nelle varie parti del corpo: il retto ha la temperatura più costante rispetto all'ambiente, mentre mani e piedi sono le zone che risentono più delle variazioni della temperatura ambientale. La temperatura subisce delle fluttuazioni circadiane di 0,5-0,7 °C, raggiungendo la temperatura inferiore verso le 6 di mattina ed un picco fra le 14 e le 22.
Possono modificare la temperatura corporea l'esercizio fisico (fino ai 40°), le emozioni, l'aumento o la diminuzione del metabolismo, l'assunzione di alimenti, il ciclo mestruale (la temperatura basale diminuisce durante l'ovulazione, per poi alzarsi di circa 0,5 °C: è un metodo usato per programmare le nascite)
La produzione di calore può essere “regolata” o “obbligatoria”. La termogenesi obbligatoria comprende:
- contrazione muscolare (parte dell'energia utilizzata viene dispersa come calore)
- normale metabolismo (il 70% dell'energia utilizzata viene dispersa sotto forma di calore)
- termogenesi indotta dalla dieta
La termogenesi regolata, per il mantenimento dell'omeostasi è dovuta a:
- brividi, contrazioni muscolari involontarie, inefficaci per produrre movimento, stimolate dall'ipotalamo
- termogenesi nel tessuto adiposo bruno, presente nell'uomo solo in età neonatale, che consiste nel disaccoppiamento della fosforilazione ossidativa.
La perdita di calore è dovuta essenzialmente a tre meccanismi che ci sono noti dalla fisica:
- irraggiamento, trasferimento di calore fra oggetti che non sono a contatto. Qualsiasi corpo al di sopra dello zero assoluto cede calore sotto forma di onde elettromagnetiche. Il nostro corpo cede più calore di quanto ne riceva se la temperatura ambientale è minore di quella corporea. A riposo, la quota del calore disperso per irraggiamento è del 60% circa;
- conduzione è il passaggio di calore da un corpo più caldo che si a contatto con un corpo più freddo. La quantità di calore disperso dipende dalla differenza di temperatura fra i due corpi. La conduzione ad altri oggetti è poco rilevante, mentre la conduzione all'aria rappresenta una quota del 15% del calore disperso. La conduzione è il trasferimento dell'energia cinetica delle particelle corporee all'aria: si tratta di un fenomeno autolimitato, poiché una volta che le molecole d'aria hanno la stessa energia cinetica (temperatura) di quelle corporee il passaggio di calore si arresta. Tuttavia, se sono presenti dei fenomeni convettivi, che portano via l'aria man mano che si riscalda la perdita di calore per conduzione aumenta considerevolmente. La temperatura della cute è fondamentale per la conduzione: la vasodilatazione aumenta la differenza di temperatura fra i due sistemi (aria e cute) e quindi la dispersione di calore, viceversa la vasocostrizione favorisce la conservazione di calore. I vestiti sono importanti nel limitare la dispersione di calore per conduzione e convezione, in quanto costituiscono un vero e proprio “cuscinetto d'aria” attorno al corpo, che viene allontanato con più difficoltà per convezione;
- evaporazione: per ogni grammo di acqua che evapora dal nostro corpo cediamo 0,5 kCal. Anche in assenza di sudorazione perdiamo per perspiratio insensibilis una quantità d'acqua di circa 0,5 l. A differenza della sudorazione, la perspiratio è un meccanismo che non può essere regolato, dovuto alla diffusione dell'acqua attraverso la cute e le superfici respiratorie. L'evaporazione dipende dall'umidità ambientale: maggiore è il grado di umidità minore sarà l'evaporazione. A riposo l'evaporazione risponde del 22% circa della perdita di calore. La polipnea è un meccanismo di dispersione del calore, sfruttato dagli animali che non hanno ghiandole sudoripare e ricchi di peli, che ventilano notevolmente lo spazio morto (es. cane che ansima) in modo da far evaporare l'acqua dalla superficie delle mucose.
I recettori per la temperatura sono presenti a livello della cute (recettori per caldo e freddo) e a livello dell'ipotalamo stesso (recettori di calore del liquor). L'integrazione delle informazioni sulla temperatura avviene a livello dell'ipotalamo anteriore per le risposte al caldo e a livello dell'ipotalamo posteriore per le risposte al freddo.
Riflessi termoregolatori
variazione della temperatura esterna variazione delle temperatura dell'ipotalamo

termocettori periferici cutanei termocettori centrali

centro integratore ipotalamo

risposta all'aumento della risposta all'abbassamento della
 temperatura temperatura
temperatura temperatura
stimolazione neuroni stimolazione neuroni stimolazione neuroni
simpatici colinergici simpatici adrenergici motori somatici

ghiandole sudoripare vasi cutanei vasi cutanei grasso bruno muscoli scheletrici
secrezione di sudore dilatazione costrizione termogenesi termogenesi
 senza brivido con brivido
senza brivido con brivido evaporazione irraggiamento
evaporazione irraggiamentocalore trattenuto produzione di calore
altri meccanismi:
Massimizzare la perdita di calore |
Minimizzare la perdita di calore |
- dilatazione dei vasi cutanei |
- vasocostrizione e piloerezione (poco efficace) |
Minimizzare la produzione di calore |
Massimizzare la produzione di calore |
- diminuisce l'apporto di cibo (TID) |
- termogenesi con brivido |
Risultato: in entrambi i casi---> omeostasi.
Regolazione dell'assunzione di cibo
Anche l'assunzione di cibo è un servomeccanismo controllato a livello ipotalamico. L'assunzione di cibo è regolata da meccanismi a breve termine, su base giornaliera, e da meccanismi a lungo termine, basati sul peso corporeo.
Tale meccanismo è regolato da due centri ipotalamici:
- il centro della fame, sito nell'ipotalamo laterale, tonicamente attivo. La sua stimolazione dà ingestione di cibo, mentre la sua distruzione provoca anoressia e morte. Il centro della fame viene inibito in maniera transitoria dall'altro
- centro della sazietà, corrispondente al nucleo ventromediale. Se stimolato va ad inibire il centro della fame: la sua distruzione provoca obesità.
Sono state proposte 4 ipotesi principali sui meccanismi che controllano l'assunzione di cibo da parte dell'ipotalamo. Le quattro ipotesi, che non si escludono necessariamente fra loro, sono:
- ipotesi lipostatica: il tessuto adiposo produce un segnale umorale, la leptina, una proteina circolante di 167 aa. La leptina agisce tramite il neuropeptide cerebrale Y, riducendone l'espressione genica ed anche la sensibilità da parte dell'ipotalamo laterale e mediale. Il neuropeptide Y, prodotto nel nucleo arcuato, agisce sui centri della fame e della sazietà aumentando l'apporto di cibo. La leptina, diminuendone l'espressione, stimola la sensazione di sazietà. La stretta collaborazione fra leptina e neuropeptide Y è dimostrata dal fatto che topi knock-out per il gene ob, che codifica per la leptina, riducono la loro assunzione di cibo solo se è inattivato anche il gene per il neuropeptide Y, ripsetto ai topi ob/ob (obesi). Anche i topi con inattivazione del recettore per la leptina, db, sono obesi.
- ipotesi glucostatica: si ritiene che il centro della sazietà sia sensibile alla concentrazione di glucosio. Quando il consumo di glucosio da parte del centro ventromediale è basso, questo si inattiva e permette al centro della fame di scaricare tonicamente. Questa ipotesi è supportata da alcune osservazioni sperimentali. Sostanze che riducono l'utilizzo di glucosio (2-desossiglucosio) a livello delle cellule, iniettate nei ventricoli, stimolano la fame. Nel diabete mellito, in cui l'utilizzazione cellulare del glucosio è ridotta, si ha polifagia.
- ipotesi del peptide gastrointestinale: si ritiene che l'assunzione di cibo provochi il rilascio a livello del tubo gastrointestinale di alcuni peptidi, che agiscono sull'ipotalamo inibendo l'assunzione di alimenti. Tra i polipeptidi coinvolti sembrano esserci CCK e GLP-1, i cui recettori sono presenti a livello ipotalamico. L'iniezione di questi peptidi a livello ventricolare inibisce l'assunzione di alimenti, tuttavia il ruolo di questi peptidi deve essere ancora studiato più approfonditamente per definirli come regolatori dell'appetito.
- ipotesi termostatica: l'assunzione di cibo è maggiore nei luoghi freddi e ridotta negli ambienti freddi; tuttavia vi sono poche prove che la temperatura sia un regolatore dell'appetito.
Anche la masticazione e la deglutizione generano sazietà, così come la distensione delle pareti dello stomaco. La vista, l'odore del cibo e la contrazione delle pareti gastriche provocano invece un aumento dell'appetito.
La regolazione dell'assunzione di cibo è in buona parte encefalizzata, per cui risponde a fattori sociali, ambientali e psicologici. Si è calcolato che questi ultimi possono influire per il 30% circa nell'assunzione di cibo. L'appetito non è encefalizzato negli animali, dove è quasi esclusivamente sotto il controllo ipotalamico: per questo negli animali non si riscontrano casi di obesità o di anoressia che abbiano cause diverse da quelle fisiche.
L'assunzione di cibo è finemente regolata nell'uomo, tuttavia il peso corporeo aumenta con l'età. Si è calcolato che tale aumento di peso è dovuto ad uno squilibrio fra l'assunzione di cibo ed il dispendio energetico di solo uno 0,03%.
Regolazione dell'osmolarità del LEC (meccanismo della sete). Anche il meccanismo della sete è sotto il controllo ipotalamico, come dimostrano alcune lesioni che possono diminuire o aumentare l'assunzione di acqua.
Una riduzione dell'apporto di acqua provoca un aumento dell'osmolarità del LEC. Sembra che nell'ipotalamo siano presenti degli osmocettori, che innescano il meccanismo della sete per mantenere l'omeostasi.
Un altro effetto del ridotto apporto di acqua è la riduzione del volume plasmatico. La variazione di questo parametro viene rilevata da barocettori e volocettori a livello del circolo venoso e nell'atrio destro. La riduzione del volume plasmatico provoca inoltre la liberazione di renina da parte del rene. La renina agisce sull'angiotensinogeno per produrre angiotensina I, che viene idrolizzata ad angiotensina II. L'angiotensina II stimola la sete agendo sui recettori localizzati a livello dell'organo sottofornicale, area recettrice specializzata del diencefalo. L'angiotensina II inoltre provoca vasocostrizione, liberazione di aldosterone e ADH.
La secchezza della faringe provoca sete. Nella sete sono coinvolti anche fattori psicologici e sociali.
Gli animali disidratati sono in grado di assumere una quantità d'acqua in quantità esattamente sufficiente a compensare il deficit. Poiché essi smettono di bere prima che l'acqua sia assorbita, è evidente che vi deve essere un meccanismo di misura a livello faringeo o gastrointestinale. Un meccanismo del genere, ma meno efficace, sembra essere presente anche nell'uomo.
Funzioni endocrine dell'ipotalamo: sistema neuro-endocrino
In quasi tutti i mammiferi i due ormoni secreti dall'ipofisi posteriore sono la vasopressina (o ormone antidiuretico, ADH) e l'ossitocina. Gli ormoni dell'ipofisi posteriore sono sintetizzati nei corpi cellulari dei neuroni magnocellulari presenti nei nuclei sopraottico e paraventricolare e trasportati all'ipofisi posteriore lungo i loro assoni, che formano il fascio ipotalamo-ipofisiario. A livello dell'ipofisi posteriore vengono secreti in risposta all'attività elettrica della terminazioni. Ossitocina e vasopressina vengono definiti neurormoni, cioè ormoni secreti in circolo da cellule nervose.
La sintesi dei neurormoni avviene a partire da molecole precursori più grandi. Il precursore della vasopressina prende il nome di prepro-pressofisina, ed è costituito da una sequenza segnale, neurofisina I, vasopressina e un glicopeptide. La prepro-ossifisina è costituita dalla sequenza segnale, neurofisina II e ossitocina.
Le molecole dei precursori vengono sintetizzate a livello dei ribosomi, poi a livello del reticolo endoplasmatico le sequenze segnale vengono rimosse e le molecole vengono impacchettate in vescicole. Le vescicole giungono tramite flusso assoplasmatico all'ipofisi posteriore. Durante il trasporto avviene la scissione fra neurofisine ed ormoni. I granuli di deposito a livello dell'ipofisi contengono così ossitocina e vasopressina, ma anche le neurofisine ed il glicopeptide, le cui funzioni sono ancora ignote. Gli ormoni vengono depositati in granuli a livello delle terminazioni nervose: l'arrivo di un potenziale d'azione ne provoca il rilascio mediante esocitosi Ca-dipendente.
La scarica dei neuroni che producono vasopressina è diversa dalla scarica dei neuroni che producono ossitocina. La stimolazione di questi ultimi – dovuta ad es. ad una stimolazione del capezzolo – produce una scarica sincrona, ad alta frequenza, dopo un breve periodo di latenza. Tale scarica è relativamente breve. Un'emorragia, invece, provoca – a livello dei neuroni vasopressinici – una scarica fasica, non sincrona nei vari neuroni secernenti vasopressina. Tale scarica è più prolungata ed è più idonea per mantenere un elevato livello di vasopressina più a lungo.
Gli effetti della vasopressina sono dovuti alla sua azione su tre diversi tipi di recettori, tutti legati a proteine G:
- il recettore V2 media l'inserimento di acquaporine a livello del dotto collettore. È responsabile dell'aumento di riassorbimento facoltativo di acqua (effetto antidiuretico);
- il recettore V1A è presente nel muscolo liscio vasale ed è responsabile dell'effetto vasocostrittorio della vasopressina
- il recettore V1B è specifico dell'ipofisi anteriore, dove media l'aumento di secrezione di ACTH.
Gli stimoli che aumentano la scarica dei neuroni vasopressinici sono:
- aumentata pressione osmotica del plasma
- diminuzione del volume del LEC
- dolore, emozione, stress, attività fisica
- angiotensina II
È ancora incerto se gli osmocettori che mediano i meccanismi della sete sono gli stessi che mediano il rilascio di vasopressina.
La diminuzione della pressione osmotica e aumento del volume del LEC diminuiscono la secrezione di vasopressina. Effetto analogo ha anche l'alcol etilico.
Si chiama diabete insipido una patologia dovuta alla carenza di vasopressina o alla manca risposta da parte del suo organo bersaglio, i reni. La malattia può essere dovuta ad un tumore ipofisiario, a cause traumatiche, oppure a mutazioni nel gene per la vasopressina. I pazienti soffrono di poliuria (aumento della quantità di urina escreta) e di polidipsia (aumento della quantità d'acqua ingerita), se il meccanismo della sete è ancora intatto. È proprio il meccanismo della sete che mantiene in vita questi pazienti, poiché se venisse a mancare potrebbero andare incontro ad una disidratazione fatale.
Il diabete insipido nefrogeno è dovuto alla mancata risposta dei reni alla vasopressina. Questa patologia è legata a difetti nel recettore V2 per la vasopressina, oppure ad una forma non funzionale dell'acquaporina che viene inserita a livello del dotto collettore (acquaporina 2) in seguito a stimolazione della vasopressina.
L'ossitocina agisce principalmente a livello dell'utero e della ghiandola mammaria. A livello della ghiandola mammaria l'ossitocina provoca la contrazione di cellule mioepiteliali, cellule simili alle cellule muscolari che tappezzano i dotti della ghiandola mammaria. Il riflesso di eiezione del latte viene provocato dalla stimolazione dei recettori tattili abbondanti nel capezzolo e nel petto. Gli impulsi seguono le vie della sensibilità somatica tattile fino al nucleo sopraottico e paraventricolare, dove stimolano il rilascio di ossitocina. L'ossitocina giunge a livello della ghiandola mammaria, dove stimola la contrazione delle cellule mioepiteliali e provoca l'eiezione del latte.
L'ossitocina stimola anche le contrazioni uterine durante il parto. I recettori tattili aumentano notevolmente di numero prima del parto ed avviano le contrazioni uterine. Il passaggio del feto attraverso il canale genitale stimola ulteriormente i recettori, provocando un feedback positivo: gli impulsi vengono trasmessi ai nuclei sopraottico e paraventricolare che secernono una quantità maggiore di ossitocina.
L'ossitocina potrebbe favorire nella donna non gravida la risalita dello sperma nell'utero, ma sono necessarie maggiori evidenze sperimentali. Nell'uomo il ruolo dell'ossitocina sembra essere quello di far contrarre i vasi deferenti, spingendo lo sperma verso l'uretra.
Veglia e sonno
Il sonno è una sospensione dello stato di coscienza, accompagnata da un'attività elettrica cerebrale specifica, con onde cerebrali caratteristiche. Occupa circa un terzo della nostra vita, ed è presente in tutti i mammiferi. L'astinenza completa dal sonno è mortale. Le ore di sonno variano con l'età: 16 per i neonati, 9 ore per gli adolescenti, 7,5 ore per gli adulti. Il debito di sonno provoca riduzione dei riflessi, ridotta capacità di giudizio e di memoria, sbalzi d'umore, allucinazioni. La massima privazione del sonno finora registrata è stata di 264 ore (11 giorni).
Ancora non è chiaro il motivo per cui dormiamo: forse per ripristinare il livello di glucosio nel cervello o per “riazzerarare” la macchina cerebrale, il cui uso prolungato porta ad una diminuita capacità operazionale.
Il sonno è una delle manifestazioni più evidenti del ritmo circadiano. Il ciclo sonno-veglia ha una durata di 26 ore, se il soggetto è privo di informazioni temporali; tuttavia tale ciclo è in grado di sincronizzarsi con l'alternarsi del ciclo giorno/notte e si riduce a 24 ore. Tale meccanismo di sincronizzazione è in relazione con alcuni recettori della luce presenti nella retina. Tali recettori sono diversi dai coni e dai bastoncelli; si trovano nello strato delle cellule gangliari ed amacrine ed utilizzano il fotopigmento melnopsina. I recettori proiettano al nucleo soprachiasmatico dell'ipotalamo (il nostro orologio biologico, che è settato su un ciclo di 26 ore). L'ipotalamo proietta ai neuroni simpatici pregangliari delle corna laterali del midollo spinale; i neuroni postgangliari, siti nei gangli cervicali superiori, si portano all'epifisi. Quest'ultima libera melatonina, ormone che modula l'attività dei circuiti del tronco encefalico che controllano il sonno e la veglia.
Formazione reticolare. La formazione reticolare è un nucleo filogeneticamente molto antico che si trova nella porzione ventro-mediale del bulbo e del mesencefalo. Si tratta di una rete molto complessa di neuroni, con funzioni diverse e non ben definiti anatomicamente. Manca la suddivisione in sostanza bianca e sostanza grigia, e si parla di centri della formazione reticolare solo in senso fisiologico. Le funzioni della formazione reticolare sono diverse, fra cui:
- regolazione della funzione cardiocircolatoria e respiratoria
- mantenimento del tono muscolare (tramite il fascio reticolo-spinale)
- controllo dell'attività dei motoneuroni γ
- mantenimento dello stato di veglia (sistema reticolare attivatore)
- comportamento istintivo ed emozionale
i neuroni coinvolti nella regolazione del ciclo sonno-veglia sono i neuroni colinergici nella giunzione ponte-mesencefalo, i neuroni adrenergici del locus ceruleus ed i nuclei del rafe, serotoninergici.
La formazione reticolare riceve afferenze da tutte le vie sensitive. La complessità del sistema e l'alto grado di convegenza rendono il sistema aspecifico, in quanto viene attivato allo stesso modo da differenti stimoli sensoriali, a differenza delle vie sensoriali classiche, che sono altamente specifiche. Le efferenze della formazione reticolare si portano diffusamente alla corteccia, attraverso i nuclei intralaminari del talamo. Secondo alcuni esistono anche delle fibre dirette dalla formazione reticolare alla corteccia.
Il ruolo della formazione reticolare è evidente studiando i potenziali evocati. Si tratta di fenomeni elettrici corticali, che conseguono alla stimolazione di una via sensitiva. Vengono misurati con due elettrodi, un elettrodo esplorante ed uno indifferente, nell'animale anestetizzato (in modo da ridurre l'attività elettrica di base; i potenziali evocati sono presenti anche nell'animale sveglio e possono essere riconosciuti dopo molte misurazioni, eliminando algebricamente l'attività di base).
Stimolando un nervo sensitivo si ha – dopo 5-12 ms – un'onda superficie-positiva, seguita da una piccola onda negativa, che insieme prendono il nome di potenziale evocato primario. Tale potenziale viene rilevato solo in corrispondenza della zona di arrivo delle vie provenienti dall'organo stimolato; con i potenziali evocati primari è stato infatti possibile mappare la corteccia motoria. Dopo il potenziale primario (20-80ms dopo la stimolazione) si sviluppa una seconda onda, positiva, più ampia. Tale onda è il potenziale evocato diffuso e, a differenza del potenziale primario, è rilevabile in quasi tutte le zone corticali e in molte parti del cervello. Il potenziale evocato diffuso viene rilevato anche dopo una sezione circolare che separa la zona di insorgenza del potenziale primario, il che sta ad indicare che il potenziale non è dovuto ad una semplice propagazione laterale, ma proviene da un sistema inferiore, che proietta diffusamente su tutta la corteccia (si tratta proprio dei nuclei intralaminari del talamo).
È possibile rilevare l'attività elettrica di fondo del cervello utilizzando elettrodi applicati sulla scatola cranica (o talvolta sulla superficie piale della corteccia). Tale registrazione prende il nome di elettroencefalogramma (o di elettrocorticogramma, se gli elettrodi sono applicati direttamente sulla superficie piale. L'ampiezza delle onde in questo caso è maggiore, ma è poco utilizzato). La misurazione dell'elettroencefalogramma può essere bipolare o unipolare: la prima misura le variazioni di potenziale a fra due elettrodi posti sulla scatola cranica; la seconda fra un elettrodo messo sulla scatola cranica ed uno – in teoria elettricamente indifferente – piazzato in una zona del corpo distante dalla corteccia.
Nell'adulto a riposo, con la mente rilassata e gli occhi chiusi, la componente più importante dell'EEG prende il nome di ritmo alfa, una serie abbastanza regolare di onde con un ampiezza di 50-100 microvolt ed una frequenza di 8-12 Hz. Oltre al ritmo alfa vengono descritti anche
- un ritmo beta, con onde meno ampie e più frequenti (18-30 Hz). Viene rilevato se il soggetto apre gli occhi, nella regione frontale;
- un ritmo theta, con onde ampie e frequenza di 4-7 Hz;
- un ritmo delta, con onde ampie e a frequenza inferiore a 4 Hz, tipico del sonno profondo.
Se si punta l'attenzione su qualcosa il ritmo viene interrotto da un'attività di basso voltaggio e ad alta frequenza. Tale attività viene definita come risposta di risveglio o di allerta, poiché corrisponde a questi stati corticali. Viene anche chiamato desincronizzazione, per l'aspetto irregolare; si tratta tuttavia di una apparenza, poiché anche l'attività desincronizzata è “sincronizzata”, ma ad un livello più complesso.
Il sonno non è un fenomeno unitario: esistono due tipi di sonno, il sonno REM ed il sonno non-REM (NREM). Il sonno NREM viene suddiviso in quattro fasi:
- onde con frequenza elevata e bassa ampiezza: è lo stadio dell'assopimento (onde alfa frammiste ad onde theta)
- è uguale al precedente, ma compaiono i fusi del sonno, gruppi di onde alfa-simili
- la frequenza si abbassa e l'ampiezza aumenta: sonno moderato (onde delta + fusi)
- le onde sono più ampie e a frequenza ridotta ( solo ritmo delta): è la fase del sonno più profondo
Le fasi del sonno durano circa 60 minuti, dopodiché si ritorna spontaneamente alla fase III, poi alla fase II, quindi si passa al sonno REM. Durante il sonno REM l'attività EEGrafica è aumentata; le onde ampie e regolari del sonno NREM (definito anche sonno ad onde lente) fanno spazio ad un'attività ad alta frequenza e ampiezza ridotta, che assomiglia a quella della fase I. La soglia per il risveglio, stranamente, risulta innalzata durante questa attività, per questo si parla di sonno paradossale. Il sonno REM è caratterizzato da una marcata riduzione del tono muscolare (dovuta all'attività del locus ceruleus) e da movimenti rapidi ed irregolari degli occhi, in inglese rapid eye moviment (REM). Altra caratteristica del sonno REM sono dei potenziali fasici, in gruppi di 3-5, che originano dal ponte e passano al corpo genicolato laterale ed alla corteccia occipitale. Sono chiamati potenziali ponto-genicolo-occipitali e sono forse collegati con l'attività onirica. Durante il sonno REM si hanno allucinazioni visive, un maggior livello emotivo: il cervello è attivo in un corpo inattivo (al contrario, nel sonno NREM, il cervello è inattivo in un corpo attivo). La fase REM dura circa 10 minuti, dopo si riprende il ciclo, dalla fase I alla IV e poi fase REM. In una notte, si alternano 5 fasi REM ad altrettante fasi non-REM. Il risveglio mattutino avviene solitamente durante la fase REM.
Genesi delle attività elettriche ritmiche. L'attività di una zona corticale tende ad inibire l'attività delle zone contigue. Per registrare un'attività ritmica è necessario che sia presente un centro in grado di sincronizzare la scarica di migliaia (talvolta milioni) di neuroni.
Le onde alfa non si manifestano se la corteccia non è connessa verso il talamo. Inoltre se vengono stimolati i nuclei intralaminari del talamo o la formazione reticolare, si ha un'attività elettricha ritmica, con una frequenza di 8-13 Hz, cioè la frequenza del ritmo alfa. Ciò ha fatto ritenere che il responsabile della genesi del ritmo alfa sia il talamo, con il suo sistema di proiezione aspecifica, probabilmente attivato dalla formazione reticolare.
Il sonno ad onde lente non è invece generato da vie che transitano per il talamo: una sezione delle fibre talamo-corticali non influisce sulla generazione di onde delta, mentre blocca le onde alfa. Il sonno ad onde lente si genera in seguito a stimolazione di tre aree:
- nuclei serotoninergici del rafe, che proiettano diffusamente alla neocorteccia, al talamo, alla formazione reticolare;
- nucleo del tratto solitario, che sembra agire attraverso l'attivazione del sistema serotoninergico
- alcune aree del diencefalo
Meccanismi che producono risveglio. Il sistema reticolare attivatore è il responsabile del risveglio. Fibre sensitive che giungono tramite vie specifiche al tronco encefalico, rilasciano fibre collaterali per la formazione reticolare, che raggiungono la corteccia tramite i nuclei intralaminari del talamo a proiezione aspecifica. Il risveglio può essere indotto tramite stimolazione di alcune zone corticali: nella scimmia la circonvoluzione temporale superiore e le regioni orbitali del lobo frontale. La stimolazione di altre zone dà scarsi risultati, anche se la stimolazione è di una certa intensità. Ciò fa supporre la presenza di fibre corticofughe, che si portano dalla corteccia alla formazione reticolare. Queste fibre sono le stesse che probabilmente mediano la risposta generalizzata d'allerta a stimoli psichici ed emotivi.
Funzioni sensitive del SN
Classificazione forme sensibilità
Le informazioni sensoriali che ci arrivano dall'interno e dall'esterno del corpo possono essere distinte in coscienti ed incoscienti, a seconda se raggiungono o meno il livello di coscienza corticale. I sensi coscienti sono i sensi speciali, i sensi somatici ed i sensi viscerali:
- speciali: vista, udito, olfatto, gusto, accelerazione rotatoria e lineare (equilibrio)
- somatici: tatto, pressione, freddo, caldo, dolore (sensi cutanei)
propriocezione (posizione del corpo nello spazio)
- viscerali: dolore viscerale
I sensi non coscienti sono: la lunghezza dei muscoli, la tensione dei muscoli, la pressione arteriosa, la pressione venosa, la distensione polmonare, la temperatura sanguigna nella testa, la pressione parziale dell'ossigeno, il pH, la pressione osmotica del plasma.
I recettori possono essere suddivisi in base alla natura degli stimoli ai quali rispondono.
I meccanocettori rispondono a stimoli meccanici lievi (accarezzamento) o intensi (deformazione) e possono essere differenziati in meccanocettori a rapido adattamento o a lento adattamento.
I meccanocettori a rapido adattamento sono i recettori dei follicoli piliferi, i corpuscoli di Meissner della cute glabra e i corpuscoli di Pacini del tessuto sottocutaneo.
I recettori dei follicoli piliferi e i corpuscoli di Meissner rispondono meglio a frequenze di 30-40 Hz e sentono gli oggetti ruvidi; i corpuscoli di Pacini rispondono preferenzialmente a stimoli di 250 Hz: distinguono le varie superfici.
I meccanocettori a lento adattamento sono rappresentati dai dischi di Merkel e dai corpuscoli di Ruffini. I dischi di Merkel hanno campi recettivi puntiformi e permettono di distinguere forme e margini. I corpuscoli di Ruffini si trovano nella cute, nelle articolazioni, nei tendini e la loro funzione – ancora non chiara – sembra quella di rispondere allo stiramento di una regione cutanea (anche ad una certa distanza da un recettore).
Gli assoni di tutti i meccanocettori sono mielinizzati: la maggior parte di essi sono fibre Aβ. Ultimamente sono stati descritti anche recettori innervati da fibre amieliniche (fibre C).
I termorecettori sono in grado di sentire le diverse gradazioni di temperatura: gelo, freddo, fresco, indifferenza termica, caldo, caldo intenso, caldo urente. Esistono due tipi di recettori: i termocettori sensibili al caldo ed i termocettori sensibili al freddo. Entrambi i tipi di recettori sono a lento adattamento. Sono localizzati al di sotto dell'epidermide; sono più numerosi i recettori per il caldo. I recettori per il caldo hanno un'attività spontanea anche in condizioni normali. Sono dotati di un adattamento medio-alto, che si verifica fra i 20° e i 40°. I recettori per il freddo scaricano fra i 20° e i 25°; i recettori per il caldo fra i 40° ed i 45°. Le fibre dei recettori per il freddo sono piccole fibre amieliniche (Aδ), quelle dei recettori per il caldo sono fibre mieliniche (C).
Nella percezione del caldo urente e del gelo possono essere attivati anche recettori per il dolore (i recettori termici non trasmettono stimoli dolorifici).
I chemocettori sono i recettori sensibili alla variazione della composizione chimica del loro ambiente. Fra questi vi sono i recettori del gusto e dell'olfatto, come pure i recettori del plasma sensibili alla variazione della PO2 , del pH e dell'osmolalità.
I fotocettori sono i recettori sensibili alle onde elettromagnetiche, come i recettori della vista.
I nocicettori rispondo a stimoli che possono produrre un danno reale o potenziale all'organismo. Esistono due classi principali di nocicettori, i nocicettori meccanici e i nocicettori polimodali. I nocicettori meccanici sono innervati da fibre mieliniche Aδ e sono responsabili del dolore primario o acuto, un dolore lancinante, ben localizzato e pungente, che viene avvertito dopo 0,1 s dallo stimolo. I nocicettori polimodali fanno capo a fibre amieliniche (C). Essi rispondono a tutti gli stimoli nocivi: termici, meccanici e chimici. Sono responsabili del dolore secondario, dolore urente e pulsatile che viene avvertito dopo 1 s dall'applicazione dello stimolo. Si tratta di un dolore cronico che può essere associato a componenti emotive e funzioni vegetative come nausea e vomito.
Un altro tipo di classificazione può essere fatta distinguendo gli stimoli in base alla loro provenienza:
- telerecettori, per gli stimoli provenienti lontano dal corpo (vista, udito, olfatto)
- esterocettori, per gli stimoli provenienti dall'ambiente esterno vicino (temperatura, tatto, gusto)
- enterocettori, che sentono l'ambiente interno
- propriocettori, che informano in ogni istante sulla posizione del corpo nello spazio.
I propriocettori sono cutanei, articolari e muscolari. I recettori cutanei sono i recettori del tatto visti in precedenza; nelle articolazioni troviamo corpuscoli del Pacini, corpuscoli del Ruffini e terminazioni libere. I propriocettori muscolari, sono i fusi neuromuscolari, sensibili alla lunghezza dei muscoli, ed i corpuscoli muscolo-tendinei di Golgi, sensibili alla forza dei muscoli.
La forma di energia alla quale un dato recettore è particolarmente sensibile prende i nome di stimolo adeguato. Lo stimolo adeguato per i termorecettori è la variazione di temperatura, e non la pressione, ad esempio. Tuttavia, i recettori possono rispondere talvolta anche a stimoli diversi da quello adeguato, ma con una soglia più alta. Ad esempio i recettori della retina, sensibili alla luce visibile, possono essere stimolati da una pressione sul globo oculare; la loro soglia è maggiore rispetto ai recettori cutanei, ossia è necessaria una pressione maggiore rispetto ai recettori cutanei.
Vie nervose della sensibilità somatica cosciente
tatto-pressione discriminati (sensibilità epicritica) via spino-bulbo-talamo-corticale
propriocezione via trigeminale

caldo-freddo via spino-spino-talamo-corticale
dolore via trigeminale
tatto grossolano (sensibilità protopatica)
Via spino-bulbo-talamo-corticale o via dei cordoni posteriori o lemnisco mediale.
Il lemnisco mediale è costituito da grosse fibre nervose mieliniche, che trasmettono segnali all'encefalo a velocità comprese fra 30 e 110 m/s. Ha inoltre un'alta organizzazione spaziale delle fibre rispetto ai territori da cui provengono. Queste due caratteristiche – organizzazione spaziale e velocità – ne fanno la via d'elezione per gli stimoli che devono essere trasmessi rapidamente e con alta fedeltà spaziale.
I tipi di sensibilità trasmessi da questo sistema sono:
- sensibilità tattile epicritica (localizzazione stimolo, intensità stimolo, oggetti in movimento sulla cute)
- sensibilità pressoria fine
- sensibilità fasiche (sensibilità vibratoria)
- propriocezione
Organizzazione anatomica:
- I neurone: è il neurone a T dei gangli delle radici dorsali dei nervi spinali. Con il suo prolungamento centrifugo entra in rapporto con un recettore; il suo prolungamento centripeto si porta invece nel fascicolo gracile (mediale), se proveniente dalla parte inferiore del corpo, o nel fascicolo cuneato (laterale), se proveniente dalla perte superiore del corpo.
- II neurone: si trova a livello dei nuclei gracile o cuneato del bulbo. A livello del bulbo le fibre decussano, portandosi nella metà controlaterale a costituire il lemnisco mediale, che va dal bulbo al talamo. Lungo il percorso all'interno del tronco encefalico, alle fibre del lemnisco mediale si accollano le fibre del lemnisco trigeminale.
- III neurone: si trova all'interno del nucleo VPL del talamo e proietta all'area somestesica primaria.
immagine
L'analogo della via dei cordoni posteriori per la faccia è la via trigeminale. Anch'essa è formata da fibre veloci con una buona organizzazione spaziale. La via trigeminale che trasporta la sensibilità esterocettiva epicritica è così organizzata anatomicamente:
- I neurone: è un neurone a T del ganglio di Gasser, che con il suo prolungamento centrifugo si porta in una delle tre branche del trigemino, mentre con il suo prolungamento centripeto proietta al
- II neurone, contenuto nel nucleo pontino. Il lemnisco trigeminale a questo punto decussa e si accolla al lemnisco mediale.
- III neurone, contenuto nel nucleo VPM del talamo, proietta alla corteccia somestesica primaria.
La via trigeminale che trasporta la sensibilità propriocettiva dei muscoli masticatori è leggermente diversa, in quanto il suo neurone sensitivo di 1° ordine si trova a livello del nucleo mesencefalico.
Via spino-spino-talamo-corticale o del sistema anterolaterale o del lemnisco spinale
La via del sistema anterolaterale è formata da fibre mielinche di diametro più piccolo (4 micron) che hanno una velocità di conduzione pari alla metà o ad un terzo rispeto alle fibre della via dei cordoni posteriori (8-40 m/s). Il grado di localizzazione spaziale dei segnali è scarso, così come il grado di intensità (10-20 gradazioni contro le 100 del sistema dei cordoni posteriori). Anche la capacità di trasmettere segnali che si ripetono ad alta frequenza è scarsa.
Queste caratteristiche rendono inadatto il sistema anterolaterale a veicolare informazioni che necessitano una precisa localizzazione e grado di intensità; tuttavia questa via è in grado di trasmettere un largo spettro di modalità sensoriali che comprendono:
- sensibilità dolorifica
- sensibilità termica
- sensibilità tattile e pressoria protopatica
- sensazioni di solletico e prurito
- sensazioni sessuali
Organizzazione anatomica:
- I neurone: è il neurone a T dei gangli delle radici dorsali dei nervi spinali. Il suo prolungamento centripeto proietta al
- II neurone: contenuto all'interno delle lamine I, IV, V, e VI. Le sue fibre decussano a livello della commessura anteriore e si portano nei cordoni anteriore e laterale della sostanza bianca controlaterale. Studi di anatomia distinguono un fascio spinotalamico laterale (sensibilità termica e dolorifica) e un fascio spinotalamico anteriore (sensibilità tattile protopatica). Sono compresi nella via anterolaterale il fascio spinoreticolare (che raggiunge la sostanza reticolare) e il fascio spinotettale (che raggiunge i collicoli superiori, dove le informazioni somatiche vengono integrate con informazioni visive).
- III neurone. Contenuto all'interno del nucleo VPL del talamo, proietta alla corteccia somestesica primaria.
Per quanto riguarda la trasmissione del dolore, distinguiamo un fascio neospinotalamico ed un fascio paleospinotalamico. A livello delle corna posteriori del midollo spinale, i neuroni contenuti nella lamina I contraggono una sola sinapsi e si portano direttamente al talamo (o alla formazione reticolare). Questa è la via neospinotalamica, che trasporta il dolore rapido.
I neuroni delle lamine IV, V e VI contraggono sinapsi con altri neuroni a livello delle stesse corna posteriori, prima di formare la via ascendente. Questo numero maggiore di sinapsi riduce la velocità di conduzione, ma dall'altro canto aumenta le possibilità di modulazione e di integrazione del segnale. Questa è la via paleospinotalamica.
immagine
A livello della faccia le sensazioni trasportate dalla via spino-spino-talamo-corticale sono trasportate dal lemnisco trigeminale, così organizzato:
- I neurone: contento nel ganglio di Gasser
- II neurone: contenuto nel nucleo bulbare del trigemino, le sue fibre decussano
- III neurone: contenuto nel nucleo VPM del talamo le sue fibre si portano alla corteccia somestesica primaria.
Modulazione del dolore. Le informazioni nocicettive possono essere modulate, cioè ridotte, grazie al sistema analgesico. Il sistema analgesico è costituito dalle seguenti stazioni:
 corteccia somatosensoriale vie discendenti
corteccia somatosensoriale vie discendenti - ipotalamo (non si conosce l'esatta sequenza)
- sostanza grigia periacquedutturale del mesencefalo proiettano al bulbo
- nucleo del rafe magnum e formazione reticolare (bulbo)
- complesso di inibizione del dolore situato nelle corna posteriori
i neurotrasmettitori necessari per il corretto funzionamenti del sistema analgesico sono le encefaline e la serotonina. I neuroni che proiettano al rafe magnum liberano encefalina nelle loro terminazioni, i neuroni del rafe magnum utilizzano serotonina come trasmettitore. I neuroni del complesso di inibizione a livello delle corna posteriori liberano encefalina, che blocca per inibizione presinaptica la trasmissione del dolore primario e secondario. Si ritiene infatti che l'encefalina blocchi a livello delle corna posteriori i canali del calcio delle fibre dolorifiche afferenti. I canali del calcio voltaggio sensibili sono responsabili della liberazione del neurotrasmettitore a livello della sinapsi, per cui il loro blocco provoca inibizione presinaptica.
Disegnare oppure 48-4 guy
La sensibilità dolorifica può anche essere inibita grazie alla stimolazione tattile o alla stimolazione elettrica. La stimolazione di fibre afferenti di grosso diametro (Aβ) deprime la trasmissione di segnali dolorifici. Si tratta probabilmente ad un'inibizione laterale locale. Questo tipo di inibizione spiega perché tendiamo a strofinare le zone dolenti. L'efficacia dell'applicazione di impacchi o della tecnica dell'agopuntura è da ricercare probabilmente in questo fenomeno anch'essa.
L'elettrostimolazione si è dimostrata efficace nel trattamento del dolore. L'applicazione di elettrodi sulla cute o sulle zone da cui partono le vie analgesiche discendenti, provoca una riduzione notevole del dolore, anche di lunga durata (fino a 34 ore con pochi minuti di stimolazione).
La somministrazione di una sostanza farmacologicamente inerte (placebo) può provocare una diminuzione del dolore. Tale effetto è reale, poiché rimuove un sintomo reale. Questo fenomeno prende il nome di “effetto placebo” e pare che alla sua base vi sia un rilascio di oppioidi endogeni (encefaline ed endorfine). Un meccanismo simile sembra essere coinvolto anche nella analgesia da stress, in cui soggetti sottoposti ad uno stress intenso sentono molto di meno gli stimoli dolorifici (es. soldati in battaglia).
Dolore riferito. Spesso il dolore viene avvertito in una sede molto lontana dall'area responsabile della sua insorgenza. Tale fenomeno prende il nome di dolore riferito ed è abbastanza comune per i visceri. Spesso infatti il dolore viscerale viene riferito a regioni somatiche diverse da quelle dove insorge lo stimolo. Ne è un esempio eclatante il dolore cardiaco, che può essere avvertito su un'area molto ampia che va dalla mandibola all'epigastrio, dal braccio sinistro all'apice della scapola sinistra. Le possibili cause di tale fenomeno sono da ricercare nella convergenza tra fibre dolorifiche viscerali e fibre dolorifiche somatiche, per cui la corteccia “impara” che il dolore è proveniente dalle aree somatiche piuttosto che da quelle viscerali. Le fibre somatiche infatti, oltre ad essere più numerose, sono anche quelle stimolate più frequentemente. Il dolore viene spesso riferito a regioni dello stesso dermatomero, quindi a zone che hanno la stessa origine embriologica.
Il dolore è l'unica modalità sensoriale che è possibile percepire dai propri visceri. Il dolore viscerale differisce da quello somatico perché lesioni altamente localizzate non provocano una stimolazione intensa (ad es. si può tagliare l'intestino ad un paziente sveglio senza provocare dolore significativo). L'attivazione diffusa dei recettori dolorifici, invece, provoca a livello viscerale un dolore molto intenso. Stimoli diffusi si questo genere possono essere:
- ischemia (per accumulo di cataboliti acidi o prodotti di degenerazione tissutale)
- stimoli chimici (es. succo gastrico diffusosi in seguito ad un'ulcera)
- spasmo di viscere cavo (provoca stimolazione meccanica dei recettori, con un dolore a colica)
- iperdistensione di un viscere cavo (per stimolazione meccanica di recettori dolorifici o per una provocata ischenia)
I tessuti che non hanno terminazioni dolorifiche sono: il parenchima epatico, gli alveoli polmonari ed il tessuto nervoso.
Dolore centrale ed arto fantasma. Talvolta il dolore può manifestarsi anche se i recettori non vengono stimolati. Ciò si verifica quando si ha una lesione dei nervi periferici o delle strutture del SNC che partecipano alla elaborazione delle informazioni nocicettive. L'esempio più impressionante di questo fenomeno è la sindrome dell'arto fantasma, in cui un soggetto che ha ricevuto l'amputazione di un arto sente dolore alla parte del corpo amputata. Ciò è possibile perché le strutture che portano il dolore a livello corticale continuano a funzionare, anche se la sede dello stimolo è stata rimossa. Una lesione a livello di tali strutture viene interpretata dalla corteccia come proveniente dall'arto che è stato rimosso.
Codificazione dell'informazione sensoriale
Le informazioni somatosensitive vengono trasmesse alla corteccia tutte sotto forma di identici potenziali d'azione. Tuttavia noi siamo in grado di codificare l'informazione sensoriale, siamo cioè in grado di distinguere
- intensità
- durata
- sede
- tipo
dello stimolo.
La discriminazione dell'intensità di uno stimolo viene attuata in base alla frequenza dei potenziali di azione. La corteccia impara che tanto più è alta la frequenza, tanto più è intenso il segnale. Un segnale intenso infatti provoca un ingresso maggiore di Na, che neutralizza la carica negativa citoplasmatica, con il risultato di una depolarizzazione della trigger zone più frequente.
Anche il numero di recettori attivati è importante per riconoscere l'intensità di uno stimolo. Più recettori attivati significa più vie che portano il segnale: anche questo fenomeno viene interpretato dal cervello come uno stimolo di intensità superiore.
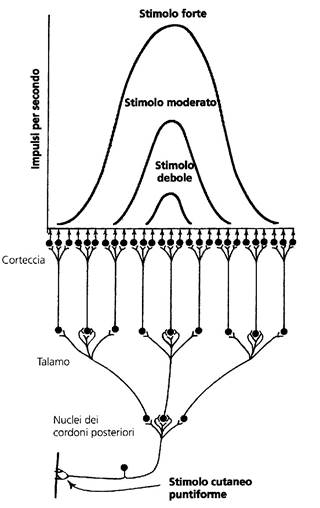 La codificazione della durata di uno stimolo dipende chiaramente dalla durata della serie dei potenziali di azione provenienti dal neurone sensoriale. Il rapporto fra la durata dello stimolo e la durata dei treni dei potenziali d'azione varia però tra un recettore e l'altro. Vi sono infatti recettori tonici, ad adattamento lento – come ad esempio quelli del dolore – che fanno sentire lo stimolo costantemente. I recettori fasici, al contrario, si adattano rapidamente alla sottrazione dello stimolo (es. recettori del tatto)
La codificazione della durata di uno stimolo dipende chiaramente dalla durata della serie dei potenziali di azione provenienti dal neurone sensoriale. Il rapporto fra la durata dello stimolo e la durata dei treni dei potenziali d'azione varia però tra un recettore e l'altro. Vi sono infatti recettori tonici, ad adattamento lento – come ad esempio quelli del dolore – che fanno sentire lo stimolo costantemente. I recettori fasici, al contrario, si adattano rapidamente alla sottrazione dello stimolo (es. recettori del tatto)
La codificazione della sede dello stimolo avviene nel seguente modo. La stimolazione di un recettore provoca la stimolazione di più neuroni a livello della corteccia, ma con frequenza diversa. Sono più stimolati i neuroni della parte centrale del campo corticale del recettore, mentre i neuroni che si trovano alla periferia del campo corticale sono meno stimolati. Il fenomeno della inibizione laterale inoltre rende più nitido il segnale. L'attivazione di una via sensitiva genera segnali inibitori laterali. Quando un neurone viene stimolato, esso trasmette il potenziale d'azione al neurone centrale e va ad inibire i neuroni laterali tramite piccoli interneuroni inibitori.
L'alta organizzazione della via dei cordoni posteriori permette alla corteccia di interpretare con precisione la provenienza dello stimolo. Per tutta la via viene mantenuta una precisa corrispondenza somatotopica: gli stimoli provenienti da una determinata regione hanno una localizzazione anatomica ben precisa. A livello corticale l'organizzazione spaziale per la ricezione dei segnali nervosi proveniente dai diversi distretti del corpo può essere efficacemente rappresentata dall'homunculus sensitivo.
 Si tratta di un disegno in cui le varie parti del corpo umano sono raffigurate accanto alla sezione della corteccia somestesica in cui sono ricevuti gli stimoli da esse provenienti. Le parti del corpo dell'homunculus non sono proporzionate alle dimensioni corporee, bensì alla densità di recettori presenti in ciascun distretto: l'homunculus ha così grandi mani, viso e labbra (ricchi di recettori) e arti e tronco piccoli (con relativamente pochi recettori).
Si tratta di un disegno in cui le varie parti del corpo umano sono raffigurate accanto alla sezione della corteccia somestesica in cui sono ricevuti gli stimoli da esse provenienti. Le parti del corpo dell'homunculus non sono proporzionate alle dimensioni corporee, bensì alla densità di recettori presenti in ciascun distretto: l'homunculus ha così grandi mani, viso e labbra (ricchi di recettori) e arti e tronco piccoli (con relativamente pochi recettori).
La discriminazione della sede di uno stimolo dipende anche dalla convergenza dei campi recettivi. Un campo recettivo è l'area somatica da cui un neurone primario rileva le informazioni. Poiché i neuroni primari sono in numero superiore rispetto ai neuroni secondari, è possibile che neuroni primari vicini convergano su uno stesso deutoneurone. Si parla allora di convergenza dei campi recettivi. Quanto più è alto il numero di neuroni convergenti, minore sarà la discriminazione.
Per misurare la sensibilità tattile si ricorre al test della discriminazione di due punti. Si applica un compasso sulla cute del soggetto bendato e gli si chiede se sente due punti distiniti di stimolazione o uno solo. Nelle zone più sensibili (punte delle dita) si riescono a distinguere stimoli a 1 mm di distanza; nelle zone meno sensibili, come ad esempio sulla cute della schiena, le punte del compasso debbono essere distanziate da 3 a 7 cm perché vengano avvertite come distinte. Ovviamente la maggiore sensibilità è dovuta ad un numero maggiori dei neuroni secondari, che minimizzano il fenomeno della convergenza.
Il tipo di stimolo (dolore, tatto, caldo, freddo) viene riconosciuto grazie alla stimolazione di colonne corticali diverse. Le colonne corticali sono unità funzionali, porzioni verticali della corteccia, costituite dai sei strati corticali.
Dermatomeri. I dermatomeri sono regioni della superficie corporea innervate da ogni nervo spinale. Esse condividono la stessa origine embriologica con il nervo spinale che le innerva. I dermatomeri sono diversi da individuo ad individuo e si sovrappongono in parte. Conoscere i dermatomeri è importante per la valutazione di pazienti neurologici, per individuare il livello della lesione spinale. Ad esempio in caso di ernia del disco è possibile capire a che livello è lo schiacciamento del disco, valutando l'insensibilità e la ridotta motilità di un dermatomero.
Perché una contrazione (attività gamma) aumenta la frequenza di scarica dei fusi?
Servoassistenza alfa-gamma
via indiretta dei circuiti dei gangli della base:un'inibizione tonica porta ad un'inibizione tonica
Fonte: http://u.jimdo.com/www400/o/s5d0ef10cc4a06ea2/download/m95ffdb01854dae7f/1281997114/Sistema+nervoso.doc
Sito web da visitare: http://infermieriuniti2.jimdo.com/area-medica/
Autore del testo: non indicato nel documento di origine
Nota : se siete l'autore del testo sopra indicato inviateci un e-mail con i vostri dati , dopo le opportune verifiche inseriremo i vostri dati o in base alla vostra eventuale richiesta rimuoveremo il testo.
Parola chiave google : Sistema motorio somatico e sistema nervoso tipo file : doc
Sistema motorio somatico e sistema nervoso
Visita la nostra pagina principale
Sistema motorio somatico e sistema nervoso
Termini d' uso e privacy