Proprietà colligative
Proprietà colligative
Questo sito utilizza cookie, anche di terze parti. Se vuoi saperne di più leggi la nostra Cookie Policy. Scorrendo questa pagina o cliccando qualunque suo elemento acconsenti all’uso dei cookie.I testi seguenti sono di proprietà dei rispettivi autori che ringraziamo per l'opportunità che ci danno di far conoscere gratuitamente a studenti , docenti e agli utenti del web i loro testi per sole finalità illustrative didattiche e scientifiche.
![]()
Proprietà colligative
Si definiscono proprietà colligative di un sistema quelle proprietà il cui valore dipende dal numero delle particelle presenti e non dalla loro natura chimica e fisica. Ad esempio la pressione ed il volume dei gas sono proprietà colligative.
Per quanto riguarda le soluzioni risultano proprietà colligative la pressione osmotica, l'abbassamento relativo della tensione di vapore nelle soluzioni, l'innalzamento ebullioscopico e l'abbassamento crioscopico.
Per esemplificare quanto detto prendiamo in considerazione la pressione osmotica.
Abbiamo visto che la pressione osmotica si calcola
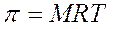
La pressione osmotica di una soluzione 0,1 M di un qualsiasi soluto a 20°C dovrebbe dunque essere pari a
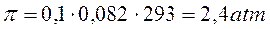
ma se misuriamo la pressione osmotica di una soluzione 0,1 M di cloruro di sodio, NaCl nelle stesse condizioni di temperatura, troviamo un valore doppio, pari a 4,8 atm.
Il fenomeno si spiega facilmente se pensiamo che il cloruro di sodio, come quasi tutti i sali, è un elettrolita forte (a = 1) ed è quindi completamente dissociato. In soluzione non si trovano dunque 0,1 moli per litro di molecole di NaCl, ma 0,1 mol/l di ioni Na+ e 0,1 mol/l di ioni Cl-, per un totale di 0,2 mol/l di particelle.
Poichè la pressione osmotica è una proprietà colligativa, il suo valore effettivo dipende dal numero di particelle effettivamente presenti, che in questo caso particolare risultano essere esattamente il doppio di quelle teoricamente immesse in soluzione.
In generale dunque per ottenere dei valori attendibili per le proprietà colligative sarà necessario moltiplicare il numero di moli teoriche per un coefficiente che ci dia il numero di particelle effettivamente presenti in soluzione.
Per trovare il numero di particelle effettivamente presenti possiamo procedere in questo modo:
supponiamo di mettere in soluzione n moli di un elettrolita E il quale si dissoci in n ioni e presenti un grado di dissociazione a.
Allora
n = numero di moli inizialmente presenti
na = numero di moli che si dissociano
n - na = numero di moli indissociate
nan = numero di ioni che si formano dalle moli dissociate
(n - na) + nan = numero di moli indissociate + numero di ioni che si formano = numero totale di particelle
Raccogliendo a fattor comune il numero di moli n inizialmente presenti si ottiene
n(1 - a + an)
La quantità (1 - a + an) è detta numero i di van't Hoff e rappresenta per l'appunto il coefficiente per cui è necessario moltiplicare il numero di moli iniziali n per ottenere il numero di particelle effettivamente presenti in soluzione.
Il numero i di van't Hoff rappresenta quindi il coefficiente per cui è necessario moltiplicare il valore teorico di una proprietà colligativa per ottenere il valore effettivo.
Fonte: http://digidownload.libero.it/quintaachimica/CHIMICA.doc
Autore del testo: non indicato nel documento di origine
Parola chiave google : Proprietà colligative tipo file : doc
Proprietà colligative
![]()
Se vuoi trovare velocemente le pagine inerenti un determinato argomento come Proprietà colligative utilizza il seguente motore di ricerca :
Visita la nostra pagina principale
Proprietà colligative
Termini d' uso e privacy